二甲基三硫
二甲基三硫(缩写:DMTS)是一种有机化合物,化学式为CH3S3CH3,它是最简单的有机三硫化物。[1][2]它是具有恶臭气味的可燃液体,其含量在万亿分之一时便可以被检测到。[3]
| 二甲基三硫 | |
|---|---|
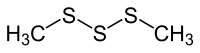 | |
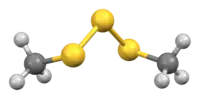 | |
| IUPAC名 (methyltrisulfanyl)methane | |
| 别名 | 2,3,4-trithiapentane |
| 识别 | |
| CAS号 | 3658-80-8 |
| PubChem | 19310 |
| ChemSpider | 18219 |
| SMILES |
|
| InChI |
|
| InChIKey | YWHLKYXPLRWGSE-UHFFFAOYAF |
| 性质 | |
| 化学式 | C2H6S3 |
| 摩尔质量 | 126.26 g/mol g·mol⁻¹ |
| 外观 | 液体 |
| 密度 | 1.1978 g/cm3 |
| 熔点 | -68.05 °C(205 K) |
| 沸点 | 170 °C(443 K) |
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |
自然存在
二甲基三硫存在于洋葱、韭菜和其他葱属物种中,以及西兰花和卷心菜释放的挥发物,还有林堡芝士也会产生它。[4]它甚至是陈年的啤酒和陈年的日本酒的香气的成分之一。[5]它是细菌分解的分解产物,包括人类尸体分解的早期阶段,[6]是麗蠅寻找宿主的主要引诱剂。二甲基三硫,以及二甲基硫醚和二甲基二硫,已经被确认为是一种名为死马海芋百合(Helicodiceros muscivorus)的吸引苍蝇的植物所释放的挥发性化合物。这些苍蝇被吸引到肉类的气味,以帮助这种植物授粉。[7]二甲基三硫是鬼笔属真菌白鬼笔发出的恶臭的成分之一,也是真菌病变的特征性恶臭,例如癌症伤口。[3]它还是人类粪便的气味成分之一。[8]
化学性质
二甲基三硫加热至80 °C(353 K),缓慢分解,得到二甲基二硫、二甲基三硫和二甲基四硫的混合物。[10]它的反应性主要体现在它的弱S-S键上(约188.3 kJ/mol)。[1]而二甲基四硫更加活泼,也包含着弱的S-S键(约150.6 kJ/mol,中心)。[10]间氯过氧苯甲酸(mCPBA)和二甲基三硫反应,得到对应的S-氧化物CH3S(O)SSCH3。[11]
参考文献
- Edward L. Clennan; Kristina L. Stensaas. . Organic Preparations and Procedures International. 1998, 30 (5): 551–600. doi:10.1080/00304949809355321.
- Ralf Steudel. . Chemical Reviews. 2002, 102 (11): 3905–3945. doi:10.1021/cr010127m.
- Shirasu, Mika; Nagai, Shunji; Hayashi, Ryuichi; Ochiai, Atsushi; Touhara, Kazushige. . Bioscience, Biotechnology, and Biochemistry. 2009, 73 (9): 2117–20. PMID 19734656. doi:10.1271/bbb.90229.
- Thomas H. Parliament; Michael G. Kolor; Donald J. Rizzo. . J. Agric. Food Chem. 1982, 30 (6): 1006–1008. doi:10.1021/jf00114a001.
- Atsuko Isogai; Ryoko Kanda; Yoshikazu Hiraga; Toshihide Nishimura; Hiroshi Iwata; Nami Goto-Yamamoto. . J. Agric. Food Chem. 2009, 57 (1): 189–195. PMID 19090758. doi:10.1021/jf802582p.
- M. Statheropoulosa; A. Agapioua; C. Spiliopoulou; G.C. Pallis; E. Sianos. . Science of The Total Environment. 2007, 385 (1-3): 221–227. doi:10.1016/j.scitotenv.2007.07.003.
- Marcus C. Stensmyr; Isabella Urru; Ignazio Collu; Malin Celander; Bill S. Hansson; Anna-Maria Angioy. . Nature. 2002, 420: 625–626. PMID 12478279. doi:10.1038/420625a.
- J.G. Moore; L.D. Jessop; D.N. Osborne DN. . Gastroenterology. 1987, 93 (6): 1321–1329. PMID 3678751.
- Mustapha Nedjma; Norbert Hoffmann. . J. Agric. Food Chem. 1996, 44 (12): 3935–3938. doi:10.1021/jf9602582.
- Timothy L. Pickering; K. J. Saunders; Arthur V. Tobolsky. . J. Am. Chem. Soc. 1967, 89 (10): 2364–2367. doi:10.1021/ja00986a021.
- J. Auger; Y. Koussourakos; E. Thibout. . Chimika Chronika. 1985, 14 (4): 263–264.
- Nilssen Arne C.; Åge Tǿmmerås Bjǿrn; Schmid Rudolf; Barli Evensen Sissel. (PDF). Entomologia Experimentalis et Applicata. 1996, 79 (2): 211–218 [2017-07-04]. doi:10.1111/j.1570-7458.1996.tb00828.x. (原始内容 (PDF)存档于2012-12-17).
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.