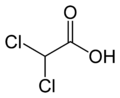
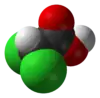
二氯乙酸
二氯乙酸(缩写:DCA)是一种有机化合物,化学式为CHCl2COOH。它是乙酸分子的甲基上的两个氢被氯取代的产物。二氯乙酸可以成盐或酯,其盐可以抑制丙酮酸脱氢酶,是一种潜在药物。[2]
| 二氯乙酸 | |||
|---|---|---|---|
| |||
| IUPAC名 Dichloroacetic acid | |||
| 别名 | Dichloroethanoic acid, bichloroacetic acid, DCA, BCA, dichloracetic acid, bichloracetic acid | ||
| 识别 | |||
| CAS号 | 79-43-6 | ||
| PubChem | 6597 | ||
| ChemSpider | 10771217 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | JXTHNDFMNIQAHM-UHFFFAOYAK | ||
| ChEBI | 36386 | ||
| RTECS | AG6125000 | ||
| DrugBank | DB08809 | ||
| KEGG | C11149 | ||
| MeSH | Dichloroacetate | ||
| 性质 | |||
| 化学式 | C2H2Cl2O2 | ||
| 摩尔质量 | 128.94 g·mol−1 | ||
| 外观 | 无色液体 | ||
| 密度 | 1.5634 g/cm3 (20 °C) | ||
| 熔点 | 9~11 °C(282~284 K) | ||
| 沸点 | 194 °C(467 K) | ||
| 溶解性(水) | 混溶 | ||
| 溶解性 | 和乙醇、乙醚混溶[1] | ||
| pKa | 1.35[1] | ||
| 磁化率 | -58.2·10−6 cm3/mol | ||
| 热力学 | |||
| ΔfHm |
−496.3 kJ·mol−1[1] | ||
| 危险性 | |||
| 警示术语 | R:R35 R50 | ||
| 安全术语 | S:S1/2 S26 S45 S61 | ||
| NFPA 704 |
 1
3
0
| ||
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |||
性质与来源
二氯乙酸的化学性质和其它卤代羧酸相似,它是氯代乙酸的一种。它和水混合时产生二氯乙酸根离子。二氯乙酸的pKa为1.35[1],纯的二氯乙酸是有机强酸;不慎吸入时可以对粘膜和上呼吸道的组织产生很大的腐蚀性和破坏性。[3]
二氯乙酸已被证明在至少一种海藻(如Asparagopsis taxiformis)中产生。[4]它可以微量存在于氯化的饮用水中,由各种含氯药物或化学品的代谢降解产生。[5]二氯乙酸通常通过还原三氯乙酸(TCA)制备。
参考文献
- Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton, FL: CRC Press. ISBN 1439855110.
- Kato, Masato; Li, Jun; Chuang, Jacinta L.; Chuang, David T. . Structure. 2007, 15 (8): 992–1004. PMC 2871385. PMID 17683942. doi:10.1016/j.str.2007.07.001.
- . Hazard.com. 1998-04-21 [2015-04-17]. (原始内容存档于2020-10-21).
- (PDF). [2017-08-08]. (原始内容存档 (PDF)于2015-04-16).
- Stacpoole, Peter W.; Henderson, George N.; Yan, Zimeng; James, Margaret O. . Environmental Health Perspectives. 1998, 106: 989–94. JSTOR 3434142. PMC 1533324. PMID 9703483. doi:10.2307/3434142.
拓展链接
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.