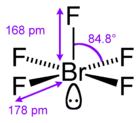
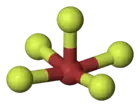
五氟化溴
五氟化溴,为溴的一种氟化物,化学式为BrF5。它是一种强氟化剂。在室温下,五氟化溴为无色液体。它的密度在0℃,100kPa下为 2.557g/L。五氟化溴的熔点为-60.6℃,沸点则为 40.9℃。
| 五氟化溴 | |||
|---|---|---|---|
 | |||
| |||
| |||
| IUPAC名 Bromine pentafloride | |||
| 识别 | |||
| CAS号 | 7789-30-2 | ||
| PubChem | 24606 | ||
| ChemSpider | 23008 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | XHVUVQAANZKEKF-UHFFFAOYAC | ||
| RTECS | EF9350000 | ||
| 性质 | |||
| 化学式 | BrF5 | ||
| 摩尔质量 | 174.894 g.mol−1 g·mol⁻¹ | ||
| 外观 | 淡黄色液体 | ||
| 密度 | 2.466 g/cm3 | ||
| 熔点 | −61.30 °C | ||
| 沸点 | 40.25 °C | ||
| 溶解性(水) | 与水反应 | ||
| 结构 | |||
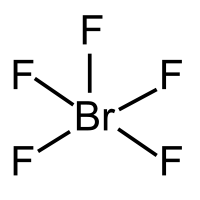
| 分子构型 | 四方锥 | ||
| 危险性 | |||
| MSDS | External MSDS | ||
| R/S术语 | R2 R23 R24 R25 | ||
| 主要危害 | 和水剧烈反应,强氧化剂[1] | ||
| NFPA 704 |
 0
4
3
| ||
| 闪点 | 不可燃 | ||
| PEL | 无[1] | ||
| 相关物质 | |||
| 其他阴离子 | 一氯化溴 | ||
| 其他阳离子 | 五氟化氯 五氟化碘 | ||
| 相关化合物 | 一氟化溴 三氟化溴 | ||
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |||
BrF5 可用于氧同位素的同位素分析。 固态硅酸盐在五氟化溴存在下的激光烧蚀释放 O2,用于后续分析。 [2] 它也已在液体火箭推进剂中作为氧化剂进行了测试,并在铀的加工中用作氟化剂。
制备
五氟化溴在1931年首次被制备。当时制备五氟化溴的方法是溴和氟直接化合。[3] 这个反应适合大规模生产五氟化溴,并是在超过150 °C(302 °F)的温度下用过量的氟气进行反应:
- Br2 + 5 F2 → 2 BrF5
- KBr + 3 F2 → KF + BrF5
反应和用处
五氟化溴和水剧烈反应,形成溴酸和氢氟酸 (特别是用乙腈进行稀释时),也就是简单的水解产物: [4]
- BrF5 + 3 H2O → HBrO3 + 5 HF
它是一种非常有效的氟化剂,能够在室温下将大多数铀化合物转化为六氟化铀。
五氟化溴可用于火箭燃料、合成中间体等。
参考资料
- NIOSH Pocket Guide to Chemical Hazards 0065
- Clayton, R.; Mayeda, T. K. . Geochimica et Cosmochimica Acta. 1963, 27 (1): 43–48. Bibcode:1963GeCoA..27...43C. doi:10.1016/0016-7037(63)90071-1.
- Hyde, G. A.; Boudakian, M. M. . Inorganic Chemistry. 1968, 7 (12): 2648–2649. doi:10.1021/ic50070a039.
- Greenwood, Norman N.; Earnshaw, Alan., 2nd, Oxford: Butterworth-Heinemann: 834, 1997, ISBN 0080379419
外部链接
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.