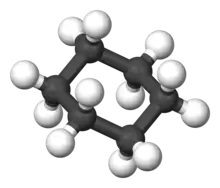
环己烷
环己烷,环烷烃的一种,也称六氢化苯。分子量:84.160。沸点:80.74℃。凝固点:6.5℃。无色,易燃,微溶于水,具有挥发性,微有刺激性气味的液体,无腐蚀性,分子式:C6H12。 作为一种重要的工业原料,环己烷主要用于合成尼龙的原料己二酸和己内酰胺。 环己烷是非极性溶剂,在涂料和清漆中有较广泛的应用。相对与苯来说环己烷毒性要小,因此在医药上用环己烷作为苯的替代溶剂。

椅型构象的环己烷分子。处于直立键的氢原子标记为红色,处于平伏键的氢原子标记为蓝色。
| 环己烷 | |||
|---|---|---|---|
| |||
| |||
| 识别 | |||
| CAS号 | 110-82-7 | ||
| PubChem | 8078 | ||
| ChemSpider | 7787 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | XDTMQSROBMDMFD-UHFFFAOYAZ | ||
| ChEBI | 29005 | ||
| DrugBank | DB03561 | ||
| KEGG | C11249 | ||
| 性质 | |||
| 化学式 | C6H12 | ||
| 摩尔质量 | 84.16 g·mol⁻¹ | ||
| 氣味 | 香,汽油味 | ||
| 密度 | 0.779 g/ml(液) | ||
| 熔点 | 6.5 °C(280 K) | ||
| 沸点 | 80.74 °C(354 K) | ||
| 溶解性(水) | 不混溶 | ||
| 折光度n D |
1.42662 | ||
| 黏度 | 1.02 cP,17 °C | ||
| 热力学 | |||
| ΔfHm |
-156 kJ/mol | ||
| ΔcHm |
-3920 kJ/mol | ||
| 危险性 | |||
欧盟危险性符号 易燃 F 易燃 F 有害 Xn 有害 Xn 危害环境N 危害环境N | |||
| 警示术语 | R:R11-R38-R65-R67 | ||
| 安全术语 | S:S2-S9-S16-S25-S33-S60-S61-S62 | ||
| NFPA 704 |
 3
1
0
| ||
| 闪点 | -20 °C | ||
| 相关物质 | |||
| 相关环烷烃 | 环戊烷、环庚烷 | ||
| 相关化学品 | 环己烯、苯、甲基环己烷 | ||
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |||
合成
工业上一般是通过苯的氢化来合成,也可以通过石油的催化重整再经分馏得到。苯催化加氢一般选择镍,钯,铂等作为催化剂,加氢反应为放热反应。通过在石油中蒸馏得到环己烷只有荷兰飞利浦公司生产。
1894年,阿道夫·冯·拜尔以庚二酸的狄克曼缩合反应开始并後接一系列还原反应合成环己烷:
同年,E. Haworth和W.H. Perkin Jr.(1860年-1929年)以1,6-二溴己烷的武兹反应开始并以相同方式合成环己烷:
令人惊奇的是,他们的合成路线最终得到的产物比环己烷沸点高10℃,这一难题於1895年由Markovnikov、N.M. Kishner和Nikolay Zelinsky解决,他们将产物烷重新确定为甲基环戊烷,是由环己烷发生意想不到的重排反应生成的。
参考资料
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.