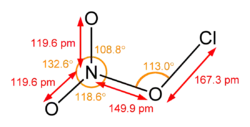
硝酸氯
它与金属、金属氯化物、醇、醚和多数有机化合物剧烈反应并可能爆炸。如果被加热到分解温度,它会释放出有毒的Cl2和NOx。
| 硝酸氯 | |||
|---|---|---|---|
| |||
 | |||
 | |||
| 系统名 Chloro nitrate | |||
| 别名 | Nitryl hypochlorite | ||
| 识别 | |||
| CAS号 | 14545-72-3 | ||
| PubChem | 114934 | ||
| ChemSpider | 102875 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | XYLGPCWDPLOBGP-UHFFFAOYSA-N | ||
| 性质 | |||
| 化学式 | ClNO3 | ||
| 摩尔质量 | 97.46 g·mol⁻¹ | ||
| 密度 | 1.65 g/cm3 | ||
| 危险性 | |||
| 欧盟分类 | |||
| NFPA 704 |
 0
3
2
| ||
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |||
硝酸氯是大气平流层中一种重要的气体。它储存着氯元素,加快臭氧的消耗。
硝酸氯与卤素或卤素互化物反应可制备其他卤素硝酸盐,如硝酸氟。与高氯酸氟类似,卤素硝酸盐也能与烯烃发生加成反应:
参考资料
- 张青莲. . 北京: 科学出版社. : P338–341. ISBN 7-03-002238-6.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.