碳-14
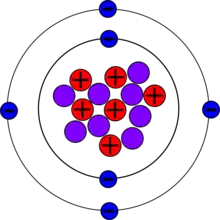
碳14(¹⁴C)或放射性碳是碳元素的一種具放射性的同位素,於1940年2月27日由加州大学伯克利分校放射性实验室(现劳伦斯伯克利国家实验室)的马丁·卡门和萨姆·鲁本首先發現。[2]它透過宇宙射線撞擊空氣中的氮原子所產生。碳-14原子核由6个质子和8个中子组成。其半衰期約為5,730±40年,衰變方式為β衰變,碳14原子轉變為氮-14原子。在地球上有99%的碳以碳-12的形式存在,有大约1%的碳以碳-13的形式存在,只有萬億分之一(0.0000000001%)是碳-14,存在于大气中。
 | |
| 基本 | |
|---|---|
| 符號 | 14C |
| 名稱 | 碳-14, C-14, 放射性碳 |
| 原子序 | 6 |
| 中子數 | 8 |
| CAS号 | 14762-75-5 |
| 核素数据 | |
| 豐度 | 萬億分之一 |
| 半衰期 | 5,730 ± 40 年 |
| 原子量 | 14.003241 u |
| 自旋 | 0+ |
| 衰變模式 | |
| 衰变类型 | 衰变能量 (MeV) |
| 貝他衰變 | 0.156476[1] |
| 碳的同位素 完整核素表 | |
1940年代,威拉得·利比在美国芝加哥大学利用碳14发明了放射性碳定年法,并于1960年获得诺贝尔化学奖。[3][4][5] 由于在有机材料中含有碳-14,因此根据它可以确定考古学、地质学和水文地质学样本的大致年代,其最大测算不超过6万年,而且没有参照的情况下誤差较大。
放射性碳定年法
由於其半衰期達5,730年,且碳是有機物的元素之一,我們可以根據死亡生物體的體內殘餘碳-14成份來推斷它的存在年齡。生物在生存的時候藉由呼吸攝入碳-14,在生物體內含量大致穩定不變,生物死去後停止呼吸,此時體內留存的碳-14因衰變開始減少。由於碳元素在自然界的各個同位素的比例一直都很穩定,人們可透過測量一件古物的碳-14含量,來估計它的大概年齡。這種方法稱之為放射性碳定年法。
这个方法估计的大气碳-14含量通过植物年轮(最多可推算到大约10000年前)或者洞穴堆积物(例如钟乳石,最多可推算到大约45000年前)来推算。根据这个推算(更确切的说)对比年轮和洞穴堆积物就可以建立起碳-14的年代变化模型,从而获得其它样本的年龄。
不過,碳-14測年法最大测算时间不超过6万年,而且所測得的年代有頗大的誤差。而且它的假定,即大氣中的碳-14濃度不會隨時間而改變,也與事實有落差。此外,碳-14測定亦有可能受到諸如火山爆發等自然因素影響,因为在火山喷发时将地下大量气体和物质带到大气中,从而影响碳-14在某区域大气中的含量。所以,若沒有其他年代測定方法(如:利用樹木的年輪)來檢訂,單單依賴碳-14的測年數據並不完全可靠。随着现代工业的高速发展和大量化石燃料的应用,古代深藏地下的碳被排放到大气中并进入生物循环,但是這些化石燃料的碳-14含量非常稀少甚至沒有,因此不會對放射性碳定年法的结果產生干擾。
存在
化石燃料中
大多数人造材料(塑料)由化石燃料,诸如石油或者煤炭制成,其中包含着远古时期的碳-14。然而,石油蕴藏物中通常存有微量的碳-14,但所含的碳-14的量不稳定,误差范围可以从当时有机物中的1%到40000年之间碳-14曾经存在过的最高水平。这表明碳-14的浓度有可能会在自然界当中受到污染,例如细菌、地下放射性物质(例如,铀元素的衰变辐射)[6] 或其它的碳-14的二次制造源。现存的碳-14在其碳质原料的同位素特征中有机会受到生物源污染或地质岩层附近环境的放射性污染。
人体中
在人体中,碳占整个身体质量的18%。生物体的每克碳内含有大约500亿个碳-14原子,其中每分钟大约有10个碳-14原子衰变。
参考文献
- Waptstra, A.H.; Audi, G.; Thibault, C. . [2007-06-03]. (原始内容存档于2008-09-23).
- . www2.lbl.gov. [2019-08-04]. (原始内容存档于2019-08-04).
- . American Chemical Society. [2019-08-04]. (原始内容存档于2019-08-04) (英语).
- . University of Chicago News. [2019-08-04]. (原始内容存档于2019-08-04) (英语).
- . NobelPrize.org. [2019-08-04]. (原始内容存档于2018-08-08) (美国英语).
- Jull, A.J.T.; Barker, D., Donahue, D. J. . Meteorics. 1985年12月, 20: 676. (abstract)
参考资料
- Bowman, Sheridan. . Berkeley: University of California Press. 1990. ISBN 0520070372.
- Currie, L. (PDF). J. Res. Natl. Inst. Stand. Technol. 2004, 109: 185–217. (原始内容 (PDF)存档于2011-02-24).
- de Vries, H. L. (1958). "Variation in Concentration of Radiocarbon with Time and Location on Earth", Proceedings Koninlijke Nederlandse Akademie Wetenschappen B, 61: 94-102; and in Researches in Geochemistry, P. H. Abelson (Ed.) (1959) Wiley, New York, p. 180.
- Friedrich, M.; et al.. . Radiocarbon. 2004, 46: 1111–1122.
- Gove, H. E. (1999) From Hiroshima to the Iceman. The Development and Applications of Accelerator Mass Spectrometry. Bristol: Institute of Physics Publishing.
- Kovar, Anton J. . American Antiquity. 1966, 31: 427–430. doi:10.2307/2694748.
- Lerman, J. C.; Mook, W. G.; Vogel, J. C.; de Waard, H. . Science. 1969, 165 (3898): 1123–1125. PMID 17779805. doi:10.1126/science.165.3898.1123. ; *Lerman, J. C., Mook, W. G., and Vogel, J. C. (1970) Proc. 12th Nobel Symp.
- Lorenz, R. D.; Jull, A. J. T.; Lunine, J. I.; Swindle, T. . Meteoritics and Planetary Science. 2002, 37: 867–874.
- Mook, W. G.; van der Plicht, J. (PDF). Radiocarbon. 1999, 41: 227–239. (原始内容存档 (PDF)于2012-05-18).
- Weart, S. (2004) The Discovery of Global Warming - Uses of Radiocarbon Dating 页面存档备份,存于.
- Willis, E.H. (1996) Radiocarbon dating in Cambridge: some personal recollections. A Worm's Eye View of the Early Days 页面存档备份,存于.
外部連結
- 黃國恩,《「碳十四測年法」的原理是什麼?》,臺灣臺東:國立臺灣史前文化博物館。
| 相邻较轻同位素: 碳-13 |
碳-14是 碳的同位素 |
相邻较重同位素: 碳-15 |
| 母同位素: 硼-14 氮-18 |
碳-14的 衰變鏈 |
衰變產物為 氮-14 |
