4-硝基苯胺
| 4-硝基苯胺 | |||
|---|---|---|---|
| |||
| 系统名 4-Nitrobenzenamine | |||
| 别名 | p-硝基苯胺 对硝基苯胺 | ||
| 识别 | |||
| CAS号 | 100-01-6 | ||
| ChemSpider | 13846959 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | TYMLOMAKGOJONV-UHFFFAOYAW | ||
| ChEBI | 17064 | ||
| 性质 | |||
| 化学式 | C6H6N2O2 | ||
| 摩尔质量 | 138.12 g/mol g·mol⁻¹ | ||
| 外观 | 黄色至棕色粉末 | ||
| 氣味 | faint, ammonia-like | ||
| 密度 | 1.437 g/cm3(固) | ||
| 熔点 | 146~149 °C(419~422 K) | ||
| 沸点 | 332 °C(605 K) | ||
| 溶解性(水) | 0.8 mg/ml at 18.5 °C (IPCS) | ||
| 蒸氣壓 | 0.00002 mmHg (20°C)[1] | ||
| 磁化率 | -66.43·10−6 cm3/mol | ||
| 危险性 | |||
| 警示术语 | R:R23/24/25 R33 R52/53 | ||
| 安全术语 | S:S28 S36/37 S45 S61 | ||
| 欧盟分类 | |||
| 主要危害 | 有毒 | ||
| NFPA 704 |
 1
2
0
| ||
| PEL | TWA 6 mg/m3 (1 ppm)(皮肤)[1] | ||
| 致死量或浓度: | |||
LD50(中位剂量) |
3249 mg/kg (rat, oral) 750 mg/kg (rat, oral) 450 mg/kg (guinea pig, oral) 810 mg/kg (mouse, oral)[2] | ||
| 相关物质 | |||
| 相关化学品 | 2-硝基苯胺, 3-硝基苯胺 | ||
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |||
合成
- ClC6H4NO2 + 2 NH3 → H2NC6H4NO2 + NH4Cl
應用
4-硝基苯胺在工業上的應用是作為重要染料成份對苯二胺的先驅物質,會再用鐵金屬及催化加氫的方式產生[3]。
4-硝基苯胺也是合成对位红(第一個偶氮染料)所需要的原料[5]:
將4-硝基苯胺置於硫酸中加熱,會快速的聚合,生成硬質的泡沬[6]。
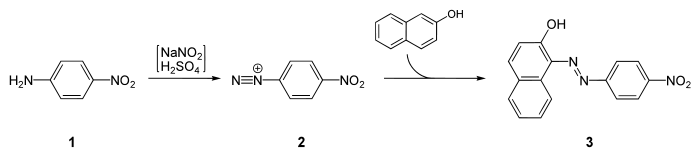
Synthesis of Para Red
實驗室應用
4-硝基苯胺有溶劑化顯色的特性,因此用來檢測卡姆列特-塔虎脫溶劑參數。其紫外-可見頻譜波峰的位置會隨溶劑中氫鍵受體及供體的平衡而變化。
参考文献
- NIOSH Pocket Guide to Chemical Hazards 0449
- . Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- Gerald Booth "Nitro Compounds, Aromatic in Ullmann's Encyclopedia of Industrial Chemistry, 7th Ed.; Wiley-VCH: Weinheim, 2005. doi:10.1002/14356007.a17_411
- Mohrig, J.R.; Morrill, T.C.; Hammond, C.N.; Neckers, D.C. "Synthesis 5: Synthesis of the Dye Para Red from Aniline." Experimental Organic Chemistry. Freeman: New York, NY, 1997; pp 456-467 页面存档备份,存于.
- Williamson, Kenneth L. . Houghton-Mifflin. 2002. ISBN 0-618-19702-8.
- . doi:10.1002/app.1970.070140813.
拓展链接
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.