DAPI
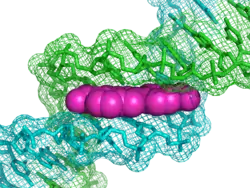
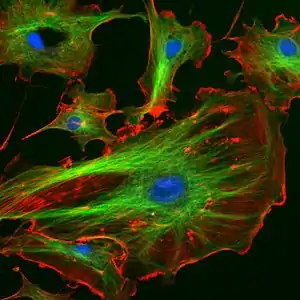
DAPI即4',6-二脒基-2-苯基吲哚(4',6-diamidino-2-phenylindole),是一種能夠與DNA強力結合的螢光染料,常用於螢光顯微鏡觀測[1]。因為DAPI可以透過完整的細胞膜[2],它可以用于活細胞和固定細胞的染色。
| DAPI | |
|---|---|
 | |
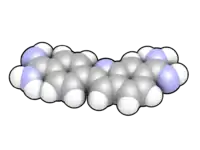 | |
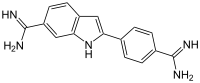
| IUPAC名 2-(4-Amidinophenyl)-1H-indole-6-carboxamidine | |
| 别名 | 4',6-Diamidino-2-phenylindole |
| 识别 | |
| CAS号 | 28718-90-3 |
| PubChem | 2954 |
| ChemSpider | 2848 |
| SMILES |
|
| InChI |
|
| InChIKey | FWBHETKCLVMNFS-UHFFFAOYAH |
| ChEBI | 51231 |
| 性质 | |
| 化学式 | C16H15N5 |
| 摩尔质量 | 277.32 g·mol−1 |
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |
历史
1971年DAPI在一项关于制抗锥虫病的药物的研究中由Otto Dann的实验室首次合成,虽然它不是一种成功的药物,但更深入的研究表明它在与DNA强力结合时发出更强的荧光,因此在1975年它被用在超速离心分析法中以标记线粒体DNA。与DNA结合时激发的强荧光使它被广泛用于荧光显微镜技术中对DNA的染色。上世纪70年代末证实DAPI可以被用来在植物,微生物,多细胞动物和细菌[3]细胞中追踪DNA,1977年证实它可以被用来定量给细胞中的DNA染色,同时也证实DAPI可在流式细胞术中用作DNA染料。[4]
荧光属性
发射与吸收波长
在螢光顯微鏡觀察下,與雙股DNA結合的DAPI染劑在358 nm(紫外线)处有一个最大吸收峰,并在461 nm(蓝)处有一个最大发射峰,其發射光的波長範圍含蓋了藍色至青綠色,因此在荧光显微技术中DAPI被紫外线照亮且被蓝或青色滤镜检出。DAPI也可以和RNA結合,但產生的螢光強度不及與DNA結合的結果,其發射光的波長範圍約在400 nm左右。[5][6][7]
DAPI的發射光為藍色,且DAPI和荧光素、綠色螢光蛋白(Green fluorescent protein, GFP)或Texas Red染劑(紅色螢光染劑)的發射波長,僅有少部分重疊,研究員可以善用這項特性在單一的樣品上進行多重螢光染色。如果需要十分精确的分析,可以使用光谱去混合(spectral unmixing)技術計算此一影响。
活细胞安全性
參考資料
- . 来邦网. [2010-01-21]. (原始内容存档于2010-01-24).
- 徐锦堂; 王黎; 周清; 杨艳; 陈剑. . 2013 [2019-05-25]. doi:10.13389/j.cnki.rao.2013.11.001. (原始内容存档于2019-09-24).
- M Cassan; E Boy; F Borne. . J Bacteriol. 1975 Aug [2019-05-13]. PMID 238953. (原始内容存档于2019-09-24).
- Kapuscinski J. . Biotech Histochem. September 1995, 70 (5): 220–33. PMID 8580206. doi:10.3109/10520299509108199.
- Scott Prahl, DAPI 页面存档备份,存于. accessed 2009-12-08.
- Kapuscinski J., 页面存档备份,存于. accessed 2013-02-25.
- Invitrogen, DAPI Nucleic Acid Stain 页面存档备份,存于. accessed 2009-12-08.
- A. Biancardi; T. Biver; F. Secco; B. Mennucci. . Phys. Chem. Chem. Phys. 2013, 15: 4596. Bibcode:2013PCCP...15.4596B. doi:10.1039/C3CP44058C.
- RUSSELL, W. C.; NEWMAN, CAROL; WILLIAMSON, D. H. . Nature. 1975, 253 (5491): 461–462. Bibcode:1975Natur.253..461R. doi:10.1038/253461a0.
- Ashraf M. Khalil. . Science. 2012 Jun 1 [2019-05-11].
- Kerenyi, Marc A; Shao, Zhen; Hsu, Yu-Jung; Guo, Guoji; Luc, Sidinh; O'Brien, Kassandra; Fujiwara, Yuko; Peng, Cong; Nguyen, Minh; Orkin, Stuart H. . eLife. 2013-06-18, 2 (2013; 2) [2019-05-11]. PMID 23795291. doi:10.7554/eLife.00633. (原始内容存档于2019-09-24).
- Zink D, Sadoni N, Stelzer E. . Methods. 2003, 29 (1): 42–50. PMID 12543070. doi:10.1016/S1046-2023(02)00289-X.
- (PDF). [2018-04-18]. (原始内容 (PDF)存档于2016-03-03).
- Slieger RF; 等. . 1980 [2019-05-25]. doi:10.13389/j.cnki.rao.2013.11.001. (原始内容存档于2019-09-24).
- Ohta T, Tokishita S, Yamagata H. . Mutat. Res. 2001, 492 (1–2): 91–7. PMID 11377248. doi:10.1016/S1383-5718(01)00155-3.
- Latt, SA; Stetten, G; Juergens, LA; Willard, HF; Scher, CD. . Journal of Histochemistry and Cytochemistry. July 1975, 23 (7): 493–505. PMID 1095650. doi:10.1177/23.7.1095650.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.