端粒
端粒(英語:)是真核生物染色體末端的DNA重複序列,作用是保持染色體的完整性和控制細胞分裂週期。 由於DNA複製的機制,每次染色體複製後,延遲股上的染色體末端必無法被複製。[1]因此,真核生物在染色體末端演化出端粒以作為可被重複遺棄的片段。[2]一旦端粒消耗殆盡,細胞將會立即啟動凋亡機制。因此,端粒被推測和細胞衰老有明顯的關係。人體的部分細胞,例如精原母細胞、癌症細胞等,含有端粒酶,能在DNA末端接上新的端粒片段,其端粒不會隨著分裂次數增加而縮短,因此能無限複製。

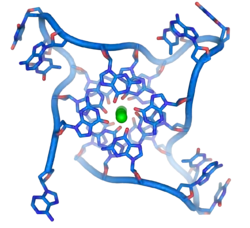
概念
端粒是存在於真核細胞線狀染色體末端的一小段DNA-蛋白質複合體,它與端粒結合蛋白一起構成了特殊的“帽子”結構,能夠維持染色體的完整和控制細胞分裂週期。
端粒DNA是由簡單的DNA高度重複序列組成的,染色體末端沿著5'到3' 方向的鏈富含 GT。在酵母和人中,端粒序列分別為C1-3A/TG1-3和TTAGGG/CCCTAA,並有許多蛋白與端粒DNA結合。端粒DNA主要功能有:第一,保護染色體不被核酸酶降解;第二,防止染色體相互融合;第三,為端粒酶提供底物,解決DNA複製的末端隱縮,保證染色體的完全複製。端粒、著絲粒和復制原點是染色體保持完整和穩定的三大要素。同時,端粒又是基因調控的特殊位點, 常可抑制位於端粒附近基因的轉錄活性(稱為端粒的位置效應,TPE)。在大多真核生物中,端粒的延長是由端粒酶催化的,另外,重組機制也介導端粒的延長。
发现和历史
结构
端粒(telomere)是由许多成串短的重复序列所组成。该重复序列通常一条链上富含G(G-rich),而其互补链上富含C(C-rich)。一个基因组内的所有端粒都是由相同的重复序列组成,但不同物种的端粒的重复序列是不同的。
| 物种 | 端粒DNA重复序列 |
|---|---|
| 酵母 | |
| Saccharomyces cerevisiae | G1-3T |
| Schizosaccharomyces pombe | G2-5TTAC |
| 原生動物 | |
| 四膜虫 | GGGGTT |
| Dictyostelium | G1-8A |
| 植物 | |
| 拟南芥(Arabidopsis) | TTTAGGG |
| 哺乳動物 | |
| 人 | TTAGGG |
例如,原生動物四膜蟲端粒的重複單位為TTGGGG(僅列一條鏈的序列);哺乳類和其他脊椎動物的端粒為TTAGGG,串聯重複500~3000次,序列長度在2kb到20kb之間不等。 TG鏈常比AC鏈更長些,形成3′單鏈末端。端粒的功能為穩定染色體末端結構,防止染色體間末端連接,並可補償滯後鏈5′末端在消除RNA引物後造成的空缺。原核生物的染色體是環狀的,其5′最末端岡崎片段的RNA引物被除去後可藉助另半圈DNA鏈向前延伸來填補。但是真核生物線性染色體在復制後,不能像原核生物那樣填補5′末端的空缺,從而會使5′末端序列從此而縮短。真核生物通過形成端粒結構來解決這個問題。複製使端粒5′末端縮短,而端粒酶(telomerase)可外加重複單位到5′末端上,結果維持端粒一定長度。
结合蛋白
端粒除了含有重複DNA序列外,還包含有特殊的「非核小體蛋白」,即端粒結合蛋白。根據該蛋白的結合特性分為兩類,一類與端粒重複序列特異性結合,在維持端粒長度方面起到重要作用[3~5],並且對端粒具有保護和調節作用[6];另一類與3′末端的單股突出結合,用於合成染色體末端的帽子結構以及調節端粒酶活性[7~9] 。
作用
- 在细胞有丝分裂的过程中,端粒会随着分裂次数的增加逐渐缩短,当端粒缩短到一定程度时便无法继续维持染色体的稳定,细胞最终死亡,故而能够根据端粒的长度预测细胞的寿命。但是在生殖细胞中,端粒的长度不随细胞分裂而缩短,推测是由于生殖细胞中富含端粒酶的缘故。
胚胎發生中,桑椹胚-胚泡转型(the morula to blastocyst transition)伴随着端粒长度的重新设定。实验建立在小鼠和牛的胚胎实验上。这些胚胎不管是来自自然受精还是体外受精,或者是由端粒已经缩短的体细胞发育而成,都有端粒长度的重新设定这一过程。
端粒酶對這一過程有重要作用,一旦缺少端粒酶,該過程就不能發生。桑椹胚-胚泡轉型是植入前發育的重要階段,能夠導致首次二細胞系分化――內細胞團(inner cell mass)和滋養層細胞(trophoblast)。端粒的長度重製能夠保證代與代之間的端粒正常,也可能和出生之後的老化與腫瘤發生有關。端粒酶,是基本的核蛋白,可將端粒DNA加至真核細胞染色體末端。端粒在不同物種細胞中對於保持染色體穩定性和細胞活性有重要作用,端粒酶能延長縮短的端粒(縮短的端粒其細胞複製能力受限),從而增強體外細胞的增殖能力。端粒酶在正常人體組織中的活性被抑制,在腫瘤中被重新激活,端粒酶可能參與惡性轉化。端粒酶在保持端粒穩定、基因組完整、細胞長期的活性和潛在的繼續增殖能力等方面有重要作用。
参考文献
- Greider C W,Blackburn E H. Identification of aspecific telomere terminal transferase activity in tetrahymena extracts. Cell ,1985 ,43 :405~4133
- Zakian A V. Telomeres :Beginning to understand the end[J ] ,Science ,1995 ,270 :1601~1607.
- Lustig A J , Stephen Kurtz ,David Shore. Involvement of the silencer and UAS binding protein RAP1 in regulation of telomere length[J ] . Science ,1990 ,250 :549~553.
- Sussel L ,David Shore. Separation of transcription activation and silencing functions of the RAP1 encoded repressor/ activator protein : Isolation of variable mutants affection both silencing and telomere length [J ] . Proc Natl Acad Sci USA ,1991 ,88 : 7749~7753.
- Nugent C I , et al . Cdc13p :A single strand telomeric DNA binding protein with a dual role in yeast telomere maintenance[J ] . Science 1996 ,274 :249~251.
- Shore D. Telomeric chromatin : replicating and wrapping up chromosome ends [ J ] . Current opinion in genetics and development ,2001 ,11 :189~198.
- Petracek M E , L M C Konkel , M L Kable and J Berman. A chlamydomonas protein that binds single2stranded G2strand telomere DNA[J ] . EMBO J ,1994 ,13 :3648~3658.
- Kim J H , Kim W T ,Chung I K. Rice proteins that bind single stranded G2rich telomere DNA [ J ] . Plant Molecular Biology ,1998 ,36 :61~672.
- Kim J H ,Kim W T , et al . Characterization and developmental expression of single2stranded telomeric DNA2binding proteins from mung bean ( V igna radiata) [J ] . Plant Molecular Biology ,2000 ,42 (4) :547~557.
- Bass H W,Marshall W F ,Sedat J W, et al . Telomeres cluster de novo before the initiation of synapsis : a three2dimensional spatial analysis of telomere positions before and during meiotic prophase [J ] . J Cell Biol ,1997 ,137 :5~18.
- Trelles Sticken E ,Loidl J .Bouquet formation in budding yeast :initiation of recombination is not required for meiotic telomere clusting[J ] . J Cell Sci ,1999 ,112 :651~658.
- De Lange T. Ending up with the right parter [J ] . Nature ,1998 ,392 :753~754.
- Hiraoka Y. Meiotic telomeres :a matchmaker for homologous chromosomes[J ] . Genes Cell ,1998 ,3 :405~413.
