利血平
利血平(英語:),或作利舍平,蛇根碱,是一种用于治疗高血压及精神病的吲哚类生物碱药物[1],最初是在萝芙木属植物蛇根木中提取而成。如今由于副作用较多并且更优的新药上市,利血平已不再是治疗的首选药物[2]。儿茶酚胺类(属于单胺类神经递质)在对心率、心肌收缩力和外周阻力的调控上起着极大作用[3],利血平的降压作用是通过消耗外周交感神经末梢的儿茶酚胺而发挥药效。
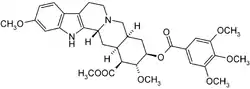 | |
| 系统(IUPAC)命名名称 | |
|---|---|
18β-(3,4,5-三甲氧基甲酰氧基)-11,17α-二甲氧基-3β,20α-育亨烷-16β-甲酸甲酯 | |
| 临床数据 | |
| 医疗法规 | |
| 妊娠分级 |
|
| 给药途径 | 口服 |
| 合法狀態 | |
| 合法状态 |
|
| 药代动力学数据 | |
| 生物利用度 | 50% |
| 代谢 | 肝脏 |
| 生物半衰期 | 分布相 = 4.5h, 消除相 = 271h, 平均 = 33h |
| 排泄 | 62% 粪便 / 8% 尿液 |
| 识别 | |
| CAS注册号 | 50-55-5 |
| ATC代码 | C02AA02 |
| PubChem | CID 5770 |
| DrugBank | APRD00472 |
| ChemSpider | 5566 |
| UNII | 8B1QWR724A |
| KEGG | D00197 |
| ChEBI | CHEBI:28487 |
| ChEMBL | CHEMBL772 |
| 化学 | |
| 化学式 | C33H40N2O9 |
| 摩尔质量 | 608.68 g/mol |
| |
| |
原料
利血平主要是从蛇根木中提取的,其中利血平含量约为0.04–0.05%[4]。此外,墨西哥的四叶萝芙木(Rauvolfia heterophylla),澳大利亚的东方狗牙花(Tabernaemontana orientalis)[5]。现今蛇根木的替代原料主要是催吐萝芙木[6],在中国也有使用云南萝芙木[7]。
历史
利血平是从蛇根木(又称印度蛇根草)[8]的干燥根中提取分离的。蛇根木在印度被称为Sarpaganda,而且多个世纪以来都被印度人用于治疗精神失常、发烧和解救蛇毒[2],就连圣雄甘地也将蛇根木作为镇静剂使用[9]。二十世纪初蛇根木中的一系列有降血压功效的生物碱被发现,其中印度人Sen和Bose于1931年发现了利血平降压和抗精神失常的作用[10][11]。1952年,埃米尔·施利特勒(Emil Schlittler)从蛇根木中分离出利血平,并于次年解析其分子结构[5][12]。1954年,在氯丙嗪问世后的两年,利血平也进入了市场,成为精神疾病治疗的常用药物之一[13] [14]。1958年,罗伯特·伯恩斯·伍德沃德完成了利血平的全合成[12][15]。
利血平同时也是一种抗高血压药物,是通过了减少高血压死亡率的随机对照试验的少数几种药物之一[16][17][18]。利血平也可用于治疗亨丁顿舞蹈症患者的运动障碍症状。[19]
由于出現大量副作用,利血平在英国早已停止使用[5][20],在1970年代后期就逐渐被其他药物替代,如甲硝利血平[20]。后来有研究表明,如果减少原用量,可在保留药效的情况下大大降低副作用的发生[21]。
利血平对神经精神药理学和现代神经精神病学的基础研究产生了非常重要的影响,虽然现在已被其他药物所替代。在1950年代至1960年代利血平的机制被深入研究,发现了许多生化过程中新的理论,如生物胺—抑郁症假说[22]。
药理作用
作用机制
利血平是一种不可逆的VMAT抑制剂。它通过阻断囊泡单胺转运体(VMAT)來产生药理作用[23]。VMAT是重要的神经递质载体,将递质储存在囊泡中并运送到细胞膜表面,随后释放到突触间隙(胞吐作用)。如果破坏VMAT的作用,突触前神经末梢产生的去甲肾上腺素、血清素、多巴胺等物质,會在未受保护的情况下被细胞质中的单胺氧化酶(MAO)以及儿茶酚邻位甲基转移酶(COMT)代谢,因而永远无法到达突触。对于交感节后神经来说,去甲肾上腺素的耗竭产生了降压作用。这种作用可能需要数天至数周才能恢复VMAT形成,因此利血平的药效是十分持久的(利血平后效应)。另外,作为一种高效抗精神病药物,它的药力是氯丙嗪的20-50倍[24]。
利血平在突触中对单胺神经递质的作用常被作为递质耗竭导致人抑郁症理论的证据。然而,这种说法有争议,有人认为利血平引发抑郁症只是天方夜谭,因为某些含有利血平的植物根部泡的茶具有的镇静安神作用可认为是一种抗抑郁作用[25]。
适应症
利血平在实际使用中的评价与标准教科书中的有很大不同,比起副作用更看重良好的耐受性[26]。当单一其他类型抗高血压药物治疗沒有效果時,低剂量利血平成为了一种良好的联合用药[27]。其他一些机构将低剂量使用含有利血平并与利尿剂合用的药物认为是一种既廉价又有效的药物[28] [29]。
利血平可用于判断和确诊癌瘤。利血平测试是一项针对于肿瘤内分泌活动的诱发试验:肿瘤会产生大量的血清素,利血平可让血清素代谢激增,于是大量的血清素降解产物5-HIAA就可在尿液中检测出[30][31]。
副作用
如同大部分抗交感神经药物,利血平也可以带来一些严重的副作用。利血平降低儿茶酚胺的有效性,从而降低交感神经张力,副交感神经佔据优势,从而导致鼻塞、噁心、呕吐、体重增加、胃部不适、胃溃疡(由于胃部胆碱能神经活动的增加并引起粘膜损伤),胃痉挛与腹泻等副作用。同时,利血平可能引起反射性心动过缓和低血压,包括姿位性低血压 [33],并可能导致哮喘恶化。鼻粘膜肿胀(由于同时浆液分泌物,所以被称为“利血平感冒)和勃起障碍也是利血平对α-受体阻滞的结果[34][27]。全身无力和疲劳也是常见副作用。
利血平使得中枢神经系统多巴胺和血清素的缺乏,引起锥体外系疾病,如帕金森氏症、嗜睡、头晕、恶梦等,并可能导致抑郁症和自殺。但利血平会导致抑郁症这一假设是依据1950年代一系列的报告得出的[35],基于现代医学研究,大部分过去的病例被误诊了,只有5-9%的患者有主要的抑郁症症状,而且他们中的大部分都有精神障碍史[36]。
利血平可能会进入母乳,或影响胎儿。利血平会影响七个月大的胎儿,使胎儿心动过缓,或使新生儿嗜睡。利血平也会引起月经问题[37]。在对啮齿类动物的高剂量给药研究发现,利血平会引起乳房纤维腺瘤和其他的恶性精囊瘤。一些早期研究表明利血平将增加(约一倍)妇女患乳腺癌的风险,但研究并未得到证实。利血平也可能导致高泌乳素血症 [34]。
利血平的副作用在低于每天0.2毫克的剂量时极少发生,最常见的是鼻塞[38]。利血平引起的抑郁症导致自杀一直备受关注。然而,这些副作用的报道是在平均每天0.5毫克的剂量的非对照试验中发现的[39][40]。
合成
参考文献
- Wayne's Word. . [2011-08-21]. (原始内容存档于2011-09-02) (英语).
- 页面存档备份,存于 The Columbia Encyclopedia, Sixth Edition. Copyright © 2001-05 Columbia University Press.
- Forney, Barbara. Reserpine for Veterinary Use 页面存档备份,存于 Wedgewood Pharmacy. 2001-2002.
- Roth, Daunderer, Kormann: Giftpflanzen – Pflanzengifte. Hüthig Jehle Rehm, 1994, ISBN 3-609-64810-4, S. 605.
- Giebelmann, von Meyer: Kulturgeschichtliches zu Hundsgiftgewächsen 页面存档备份,存于 (2003).
- Wink, van Wyk, Wink: Handbuch der giftigen und psychoaktiven Pflanzen. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2008, ISBN 3-8047-2425-6, S. 200.
- . 高等学校化学学报. 2010年4月, 31 (4): 731–735. 使用
|coauthors=需要含有|author=(帮助); - Rauwolfia 页面存档备份,存于 Dorlands Medical Dictionary. Merck Source. 2002.
- Pills for Mental Illness? 页面存档备份,存于, 时代, November 8, 1954
- Sen, Bose: Rauwolfia serpentina, a new Indian drug for insanity and high blood pressure. In: Indian Med World (1931), Vol. 2, Ss. 194–201.
- Kline: Use of Rauwolfia serpentina Benth in neuropsychiatric conditions. In: Annals of the New York Academy of Sciences (1954), Vol. 59, Ss. 107–132.
- Nicolaou, K. C.; E. J. Sorensen. . Weinheim, Germany: VCH. 1996: 55. ISBN 3-527-29284-5.
- Möller, Laux, Deister: Psychiatrie und Psychotherapie. Thieme, Stuttgart 2005, ISBN 3-13-128543-5, S. 492.
- . Actas Esp Psiquiatr. 2004, 32 (6): 387–395 [2011-08-24]. (原始内容存档于2007-09-27) (西班牙语). 使用
|coauthors=需要含有|author=(帮助) - Woodward et al.: The Total Synthesis of Reserpine. In: Tetrahedron (1958), Vol. 2, Ss. 1–57.
- ,. . JAMA. 1979, 242 (23): 2562–71. PMID 490882. doi:10.1001/jama.242.23.2562. full text at OVID
- ,. . JAMA. 1967, 202 (11): 1028–34. PMID 4862069. doi:10.1001/jama.202.11.1028.
- ,. . JAMA. 1991, 265 (24): 3255–64. PMID 2046107. doi:10.1001/jama.265.24.3255.
- Shen, Howard. . Minireview. 2008: 11. ISBN 1-59541-101-1.
- Sreemantula, Boini, Nammi: Reserpine methonitrate, a novel quaternary analogue of reserpine augments urinary excretion of VMA and 5-HIAA without affecting HVA in rats. In: BMC Pharmacology (2004), Vol. 4. Volltext 页面存档备份,存于.
- Porzig, Engelhardt: Pharmaka mit Wirkung auf das vegetative Nervensystem. In Estler, Schmidt (Hrsg.): Pharmakologie und Toxikologie. Schattauer, Stuttgart, 2006. S. 144.
- Langer: Ausschnitte einer Geschichte der Psychopharmaka im 20. Jahrhundert. In: Langer, Heimann (Hrsg.): Psychopharmaka – Grundlagen und Therapie. Springer, Wien 1983, ISBN 3-211-81746-8. Ss. 25–26.
- Henry, J.; Scherman, D. . Biochemical pharmacology. 1989, 38 (15): 2395–2404. PMID 2667522. doi:10.1016/0006-2952(89)90082-8.
- Mutschler, Geisslinger, Kreemer, Ruth, Schäfer-Körting: Mutschler Arzneimittelwirkungen kompakt. S. 72.
- Baumeister, AA; Hawkins, MF; Uzelac, SM. . Journal of the history of the neurosciences. 2003, 12 (2): 207–20. PMID 12953623.
- Starke: Pharmakologie noradrenerger und adrenerger Systeme. In: Forth, Henschler, Rummel: Allgemeine und spezielle Pharmakologie und Toxikologie. Urban & Fischer, München/Jena 2001, ISBN 3-437-42520-X, S. 206.
- Mutschler, Geisslinger, Kroemer, Ruth, Schäfer-Korting: Mutschler Arzneimittelwirkungen. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2008, ISBN 978-3-8047-1952-1, S. 357.
- Arzneimittelkommission der deutschen Ärzteschaft (Hrsg.): Arzneiverordnungen: Empfehlungen zur rationalen Pharmakotherapie. Deutscher Ärzte-Verlag, Köln 2006, ISBN 3-7691-1201-6, S. 681.
- Chobanian AV, Bakris GL, Black HR; 等. . JAMA. 2003, 289 (19): 2560–72. PMID 12748199. doi:10.1001/jama.289.19.2560. summary 页面存档备份,存于
- Kähler: Rauwolfia-Alkaloide. Boehringer Mannheim, Mannheim, 1970. Ss. 123–127.
- Roche Lexikon Medizin: Artikel Reserpin. Urban & Fischer, München 2006, ISBN 3-437-15156-8, S. 1585.
- Kähler: Rauwolfia-Alkaloide. Boehringer Mannheim, Mannheim, 1970. Ss. 108–113.
- Porzig, Häusler: Pharmaka mit Wirkung auf das vegetative Nervensystem. In: Estler (Hrsg.): Pharmakologie und Toxikologie. Schattauer, Stuttgart/New York 2000, ISBN 3-7945-1898-5, S. 96.
- AJ Giannini,HR Black. Psychiatric, Psychogenic, and Somatopsychic Disorders Handbook. Garden City,NY. Medical Examination Publishing, 1978. Pg. 233. ISBN 0-87488596-5.
- Goodwin, Ebert, Bunney: Mental effects of reserpine in man: a review. In: Shader: Psychiatric complications of medical drugs. New York, Raven Press, 1972, Ss. 73–101.
- Willner: Dopaminergic Mechanisms in Depression and Mania. In: Psychopharmacology: The Fourth Generation of Progress; Raven Press, Ltd., New York, S. 925.
- Bopp, Herbst: Handbuch Medikamente. Stiftung Warentest, 2004, ISBN 3-931908-94-1.
- Curb JD, Schneider K, Taylor JO, Maxwell M, Shulman N. . Hypertension. 1988, 11 (3 Pt 2): II51–5. PMID 3350594.
- QUETSCH RM, ACHOR RW, LITIN EM, FAUCETT RL. . Circulation. 1959, 19 (3): 366–75. PMID 13629798.
- LEMIEUX G, DAVIGNON A, GENEST J. . Canadian Medical Association journal. 1956, 74 (7): 522–6. PMC 1823144. PMID 13304797.
- Ramawat KG, Rachnana Sharma and Suri SS (1999) Medicinal Plants in : Biotechnology- Secondary metabolites (Edited by Ramawat KG and Merillon JM), pp: 366-7. Oxford and IBH, India.
- Chen, Huan: Reserpine: A challenge for total synthesis of natural products. In: Chemical Reviews, Vol. 105, Ss. 4671–4706; doi:10.1021/cr050521a.
- Gauchet, J. (1992) 页面存档备份,存于 (Synthese-Varianten im schematischen Vergleich / Englisch, pdf)
- Literaturangaben zu einigen Originalarbeiten 页面存档备份,存于 (dort ab Nr. 21)
- Stork: The Stereospecific Synthesis of Reserpine. In: Pure Applied Chemistry (1989), Vol. 61, Ss. 439–442. Siehe auch: Org. Chem. Highlights 页面存档备份,存于
外部链接
- NLM Hazardous Substances Databank – Reserpine
- PubChem Substance Summary: Reserpine 页面存档备份,存于 National Center for Biotechnology Information.
- The Stork Synthesis of (-)-Reserpine 页面存档备份,存于