细胞质基质
细胞质基质(),又称胞质溶胶()、基本细胞质(或)、透明质()[2]。为细胞质中除去细胞器和内容物以外较为均质、半透明的液态胶状物质[3]。(例如:线粒体基质将线粒体分离成许多区室)

在真核细胞中,细胞质基质被细胞膜包围,是细胞质的一部分,细胞质也包含线粒体,质体和其他细胞器(但不包括其内部液体和结构); 细胞核是分开的。 因此,细胞质基质是细胞器周围的液体基质。 在原核生物中,代谢的大部分化学反应发生在细胞质基质中,而少数发生在膜或周质空间中。 在真核生物中,虽然许多代谢途径仍然存在于细胞质基质中,但其他途径发生在细胞器内。
细胞质基质是溶解在水中的物质的复杂混合物。 尽管水构成大部分细胞质基质,但是,其在细胞内的结构和性质尚不清楚。 细胞质中钠离子和钾离子的浓度不同于细胞外液中的浓度; 这些离子水平的差异在诸如渗透压调节,细胞信号传送和可兴奋细胞,例如内分泌,神经和肌肉细胞中的动作电位的产生的过程中是重要的。 细胞质基质还含有大量的高分子,通过大分子拥挤可以改变分子的行为方式。
虽然它曾被认为是一种简单的分子溶液,但是,细胞质基质具有多种组织水平。 这些包括小分子的浓度梯度,例如钙,一起作用并参与代谢途径的酶的大复合体,以及蛋白质复合体,例如包围和分离细胞质基质部分的蛋白酶体和羧酶体。
性质和组成
细胞质基质的细胞体积比例各不相同:例如,当在细菌中这个区室形成大部分细胞结构时,在植物细胞中,主要区室是大的中央液胞[4]。 细胞质基质主要由水,溶解的离子,小分子和大的水溶性分子(如蛋白质)组成。 大多数这些非蛋白质分子的分子量小于300 Da。 这种小分子混合物非常复杂,因为参与代谢的分子(代谢产物)种类多样性是巨大的。 例如,在植物中可能产生多达200,000种不同的小分子,尽管并非所有这些小分子都存在于同一物种或单一细胞中[5] 。 单个细胞中代谢产物数量的估计预测不到1000个,例如大肠杆菌和面包酵母[6][7]。
水
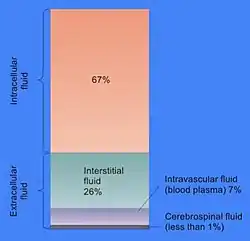
细胞质基质的大部分是水,占典型细胞总体积的70%左右[8]。 细胞内液的pH值为7.4[9] 。 而人体细胞质基质pH值范围在7.0-7.4之间,如果细胞生长则通常更高[10]。 细胞质基质的粘度与纯水大致相同,尽管小分子通过这种液体的扩散作用比纯水慢四倍,这主要是由于细胞质基质中大量高分子的碰撞[11]。 对于盐水虾的研究已经检查了水如何影响细胞功能; 他们发现细胞内水分减少20%会抑制新陈代谢,随着细胞逐渐干涸,新陈代谢活动逐渐减少,当水分低于正常值时,所有代谢活动都会停止[12]。
尽管水对生命至关重要,但细胞质基质中这种水的结构尚不清楚,主要是因为核磁共振波谱法等方法只能提供水的平均结构信息,而不能测量微观尺度的局部变化。 由于水能够通过氢键形成诸如水分子簇之类的结构,因此甚至对纯水的结构也知之甚少[13]。
对于细胞中水的经典观点是,约5%的水被溶质或大分子强烈地结合为溶剂化的水,而大多数水具有与纯水相同的结构[12]。这种溶剂化的水在渗透中没有活性,可能具有不同的溶剂性质,因此有一些溶解的分子被排除在外,而另外有一些则变得浓缩[14][15]。然而,其他人则认为细胞中高浓度大分子的影响会延伸到整个细胞质中,并且细胞中的水与稀释溶液中的水的作用非常不同[16]。这些想法包括细胞含有低密度和高密度水的区域的提议,这些区域可能对细胞其他部分的结构和功能产生广泛影响[13][17]。然而,使用先进的核磁共振波谱法方法直接测量活细胞中水的流动性与这一观点相矛盾,因为它表明85%的细胞水就像纯水一样,而其余的则不太流动,可能与大分子结合[18]。
离子
细胞质基质中其他离子的浓度与细胞外液中的浓度完全不同,并且细胞质基质还含有比细胞结构外部高得多的带电高分子,例如蛋白质和核酸。
| 离子 | 细胞质基质中的浓度 (mM) | 血液中的浓度 (mM) |
|---|---|---|
| 钾 | 139 | 4 |
| 钠 | 12 | 145 |
| 氯化物 | 4 | 116 |
| 碳酸氢盐 | 12 | 29 |
| 蛋白质中的氨基酸 | 138 | 9 |
| 镁 | 0.8 | 1.5 |
| 钙 | <0.0002 | 1.8 |
与细胞外液相反,细胞质基质具有高浓度的钾离子和低浓度的钠离子[20]。离子浓度的这种差异对于渗透压调节是至关重要的,因为如果离子水平在细胞内与外部相同,则水会通过渗透不断进入 - 因为细胞内的大分子水平高于其外部的水平。 相反,钠离子被排出并且钾离子被鈉鉀泵(Na⁺/K⁺-ATPase酶)吸收,然后钾离子通过钾选择离子通道向下流过它们的浓度梯度,这种正电荷的损失产生负膜电位。 为了平衡这种电位差,负氯离子也通过选择性氯离子通道离开细胞。 钠离子和氯离子的损失弥补了细胞内有机分子浓度较高的渗透作用[20]。
通过在细胞质中积累渗透保护剂例如甜菜碱或海藻糖,细胞可以处理更大的渗透变化[20]。 这些分子中的一些可以使细胞在完全干燥的情况下存活,并使生物体进入称为隱生的假死状态[21]。 在这种状态下,细胞溶质和渗透保护剂变成玻璃状固体,有助于稳定蛋白质和细胞膜免受干燥的破坏作用[22]。
细胞质基质中的低浓度钙允许钙离子在钙信号传送中起第二信使的作用。 在这里,诸如激素或动作电位的信号打开钙通道,使钙涌入细胞质基质[23] 。 细胞质基质钙的这种突然增加激活了其他信号分子,如钙调蛋白和蛋白激酶C[24]。 其他离子如氯化物和钾也可能在细胞质基质中具有信号传送功能,但这些并不十分清楚[25]。
大分子
那些没有与细胞膜或细胞骨架结合的蛋白质分子溶解在细胞质基质中。 细胞中的蛋白质含量非常高,接近200 mg/ml,占细胞质基质体积的20-30%[26]。 然而,准确测量蛋白质在完整细胞中溶解在细胞质基质中的程度是困难的,因为一些蛋白质似乎与整个细胞中的细胞膜或细胞器弱相关,并在细胞溶菌(lysis)后释放到溶液中[12]。实际上,在使用皂苷小心地破坏细胞质膜而不损害其他细胞膜的实验中,仅释放了约四分之一的细胞蛋白质。 如果给定ATP和氨基酸,这些细胞也能够合成蛋白质,这意味着细胞质中的许多酶与细胞骨架结合[27]。 然而,现在认为细胞中的大多数蛋白质在称为微小梁晶格的网络中紧密结合的观点是不太可能的[28]。
在原核生物中,细胞质基质包含细胞的基因组,在被称为拟核的结构中[29]。 这是一种DNA和相关蛋白质的不规则块,可控制细菌染色体和质粒的转录和复制。 在真核生物中,基因组被保持在细胞核内,细胞核通过核孔与细胞质基质分离,核孔阻止直径大于约10纳米的任何分子的自由扩散[30]。
细胞质基质中这种高浓度的大分子会产生一种称为大分子拥挤(Macromolecular crowding)的效应,即当其他大分子的有效浓度被增加,因为它们较小的体积移入。这种拥挤效应会导致细胞质中反应的化学平衡在中的速率和位置发生较大变化[26] 。 特别重要的是它能够通过促进大分子的结合来改变解离常数,例如当多种蛋白质结合在一起形成蛋白质复合体时,或者当DNA结合蛋白质与基因组中的靶标结合时[31] 。
组织
尽管细胞质基质的成分不是通过细胞膜分离成区域,但这些成分并不总是随机混合,并且几种组织层次可以将特定分子定位于细胞质基质内的确定位点[32]。
浓度梯度
尽管小分子在细胞质基质中快速扩散,但仍可在该区室内产生浓度梯度。 一个充分研究的例子是在开放的钙通道周围区域短时间内产生的“钙火花”[33]。 它们直径约为2微米,持续时间仅为几毫秒,但有几个火花可以合并形成更大的梯度,称为“钙波”[34]。 其他小分子(如氧和三磷酸腺苷)的浓度梯度可能会在线粒体簇周围的细胞中产生,尽管这些都不太了解[35][36]。
蛋白质复合体
蛋白质可以结合形成蛋白质复合体,这些蛋白质复合体通常含有一组具有相似功能的蛋白质,例如在相同代谢途径中进行多个步骤的酶[37]。该组织可以允许底物通道(Substrate channeling),即当一种酶的产物直接被通过给在代谢途径中的下一种酶而不释放到溶液中时[38] 。 如果酶在细胞质中随机分布,通道可以使代谢途径更快速和有效,并且还可以防止不稳定的反应中间体的释放[39]。 尽管各种各样的代谢途径涉及彼此紧密结合的酶,但其他代谢途径可能涉及更难以在细胞外研究的松散相关的复合体[40][41]。 因此,这些复合体在新陈代谢中的重要性一般尚不清楚。
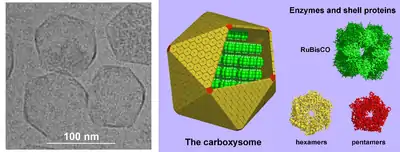
蛋白质隔室
一些蛋白质复合物含有大的中心腔,与细胞质基质的其余部分分离。 这种封闭隔室的一个例子是蛋白酶体[42]。 这里,一组亚基形成含有降解胞质蛋白的蛋白酶的空心桶。 如果它们与胞质溶胶的其余部分自由混合,这些将是被损害的,因此桶被一组调节蛋白封顶,所述调节蛋白识别具有指导它们降解的信号的蛋白质(一种泛素标签)并将它们进料到蛋白水解腔体中[43]。
另一大类蛋白质区室是细菌微区室(Bacterial microcompartment),它由包裹各种酶的蛋白质外壳制成[44]。 这些隔室通常约100-200纳米,由互锁蛋白制成[45]。 一个众所周知的例子是羧酶体,它包含碳固定中涉及的酶,如RuBisCO[46]。
功能
细胞质基质没有单一功能,而是许多个细胞过程的发生位置。 这些过程的例子包括从细胞膜到细胞内部特定位置的信号转送,如导向细胞核[51],或细胞器[52]。 在有丝分裂中核膜破裂后,细胞质基质也是细胞质分裂的许多过程的所在地[53]。细胞质基质的另一个主要功能是将代谢物从其生产地运输到使用它们的地方。 这对于水溶性分子(如氨基酸)来说相对简单,它可以通过细胞质迅速扩散[11]。然而,疏水性分子,如脂肪酸或固醇,可以通过特异性结合蛋白通过细胞质基质转送,特异性结合蛋白将这些分子在细胞膜之间穿梭[54][55]。 通过内吞作用或分泌途径进入细胞的分子也可以通过在细胞质的囊泡内被运输[56],这囊泡是被马达蛋白携带沿着细胞骨架移动的脂质小球[57]。
细胞质基质是原核生物[58]和真核生物的大部分代谢作用的发生位置。 例如,在哺乳动物中,细胞中大约一半的蛋白质被定位于细胞质基质[59]。 最完整的数据可在酵母中获得,其中代谢重建表明大部分代谢过程和代谢产物都发生在细胞质基质中[60]。 动物细胞质中发生的主要代谢途径是蛋白质生物合成,磷酸戊糖途径,糖酵解和糖异生[61]。在其他生物体中,途径的定位可以是不同的,例如植物的脂肪酸合成发生在叶绿体中[62][63],頂複門生物发生在顶质体中[64]。
参考资料
- Goodsell DS. . Trends Biochem. Sci. June 1991, 16 (6): 203–6. PMID 1891800. doi:10.1016/0968-0004(91)90083-8.
- Cammack, Richard CammackRichard; Atwood, Teresa AtwoodTeresa; Campbell, Peter CampbellPeter; Parish, Howard ParishHoward; Smith, Anthony SmithAnthony; Vella, Frank VellaFrank; Stirling, John StirlingJohn. . Oxford Dictionary of Biochemistry and Molecular Biology. Oxford University Press. 2006 [2019-08-10]. ISBN 9780198529170. doi:10.1093/acref/9780198529170.001.0001. (原始内容存档于2020-04-27) (英语).
- Brown, Thomas A. . Elsevier Health Sciences. 2011: 2 [2019-08-10]. ISBN 978-0323072601. (原始内容存档于2018-12-25) (英语).
- Bowsher CG, Tobin AK. . J. Exp. Bot. April 2001, 52 (356): 513–27. PMID 11373301. doi:10.1093/jexbot/52.356.513.
- Weckwerth W. . Annu Rev Plant Biol. 2003, 54: 669–89. PMID 14503007. doi:10.1146/annurev.arplant.54.031902.135014.
- Reed JL, Vo TD, Schilling CH, Palsson BO. . Genome Biol. 2003, 4 (9): R54. PMC 193654. PMID 12952533. doi:10.1186/gb-2003-4-9-r54.
- Förster J, Famili I, Fu P, Palsson BØ, Nielsen J. . Genome Res. February 2003, 13 (2): 244–53. PMC 420374. PMID 12566402. doi:10.1101/gr.234503.
- Luby-Phelps K. (PDF). Int. Rev. Cytol. International Review of Cytology. 2000, 192: 189–221. ISBN 978-0-12-364596-8. PMID 10553280. doi:10.1016/S0074-7696(08)60527-6. (原始内容 (PDF)存档于2011-07-19).
- Roos A, Boron WF. . Physiol. Rev. April 1981, 61 (2): 296–434. PMID 7012859. doi:10.1152/physrev.1981.61.2.296.
- Bright, G R; Fisher, GW; Rogowska, J; Taylor, DL. . The Journal of Cell Biology. 1987, 104 (4): 1019–1033. PMC 2114443. PMID 3558476. doi:10.1083/jcb.104.4.1019.
- Verkman AS. . Trends Biochem. Sci. January 2002, 27 (1): 27–33. PMID 11796221. doi:10.1016/S0968-0004(01)02003-5.
- Clegg James S. . Am. J. Physiol. 1984, 246 (2 Pt 2): R133–51. PMID 6364846. doi:10.1152/ajpregu.1984.246.2.R133.

- Wiggins PM. . Microbiol. Rev. 1 December 1990, 54 (4): 432–49 [2019-08-10]. PMC 372788. PMID 2087221. (原始内容存档于2011-06-11).
- Fulton AB. . Cell. September 1982, 30 (2): 345–7. PMID 6754085. doi:10.1016/0092-8674(82)90231-8.
- Garlid KD. . Int. Rev. Cytol. International Review of Cytology. 2000, 192: 281–302. ISBN 978-0-12-364596-8. PMID 10553283. doi:10.1016/S0074-7696(08)60530-6.
- Chaplin M. . Nat. Rev. Mol. Cell Biol. November 2006, 7 (11): 861–6. PMID 16955076. doi:10.1038/nrm2021.
- Wiggins PM. . Cell Biol. Int. June 1996, 20 (6): 429–35. PMID 8963257. doi:10.1006/cbir.1996.0054.
- Persson E, Halle B. . Proc. Natl. Acad. Sci. U.S.A. April 2008, 105 (17): 6266–71. PMC 2359779. PMID 18436650. doi:10.1073/pnas.0709585105.
- Lodish, Harvey F. . New York: Scientific American Books. 1999. ISBN 0-7167-3136-3. OCLC 174431482.
- Lang F. . J Am Coll Nutr. October 2007, 26 (5 Suppl): 613S–623S. PMID 17921474. doi:10.1080/07315724.2007.10719667.
- Sussich F, Skopec C, Brady J, Cesàro A. . Carbohydr. Res. August 2001, 334 (3): 165–76. PMID 11513823. doi:10.1016/S0008-6215(01)00189-6.
- Crowe JH, Carpenter JF, Crowe LM. . Annu. Rev. Physiol. 1998, 60: 73–103. PMID 9558455. doi:10.1146/annurev.physiol.60.1.73.
- Berridge MJ. . J. Physiol. 1 March 1997, 499 (Pt 2): 291–306 [2019-08-10]. PMC 1159305. PMID 9080360. doi:10.1113/jphysiol.1997.sp021927. (原始内容存档于2020-05-26).
- Kikkawa U, Kishimoto A, Nishizuka Y. . Annu. Rev. Biochem. 1989, 58: 31–44. PMID 2549852. doi:10.1146/annurev.bi.58.070189.000335.
- Orlov SN, Hamet P. . J. Membr. Biol. April 2006, 210 (3): 161–72. PMID 16909338. doi:10.1007/s00232-006-0857-9.
- Ellis RJ. . Trends Biochem. Sci. October 2001, 26 (10): 597–604. PMID 11590012. doi:10.1016/S0968-0004(01)01938-7.
- Hudder A, Nathanson L, Deutscher MP. . Mol. Cell. Biol. December 2003, 23 (24): 9318–26. PMC 309675. PMID 14645541. doi:10.1128/MCB.23.24.9318-9326.2003.
- Heuser J. . Biol Cell. 2002, 94 (9): 561–96. PMID 12732437. doi:10.1016/S0248-4900(02)00013-8.
- Thanbichler M, Wang S, Shapiro L. . J Cell Biochem. 2005, 96 (3): 506–21. PMID 15988757. doi:10.1002/jcb.20519.
- Peters R. . Methods Mol. Biol. Methods in Molecular Biology™. 2006, 322: 235–58. ISBN 978-1-58829-362-6. PMID 16739728. doi:10.1007/978-1-59745-000-3_17.
- Zhou HX, Rivas G, Minton AP. . Annu Rev Biophys. 2008, 37: 375–97. PMC 2826134. PMID 18573087. doi:10.1146/annurev.biophys.37.032807.125817.
- Norris V, den Blaauwen T, Cabin-Flaman A. . Microbiol. Mol. Biol. Rev. March 2007, 71 (1): 230–53. PMC 1847379. PMID 17347523. doi:10.1128/MMBR.00035-06.
- Wang SQ, Wei C, Zhao G. . Circ. Res. April 2004, 94 (8): 1011–22. PMID 15117829. doi:10.1161/01.RES.0000125883.68447.A1.
- Jaffe LF. . Cell Calcium. November 1993, 14 (10): 736–45. PMID 8131190. doi:10.1016/0143-4160(93)90099-R.
- Aw, T.Y. . Int Rev Cytol. International Review of Cytology. 2000, 192: 223–53. ISBN 978-0-12-364596-8. PMID 10553281. doi:10.1016/S0074-7696(08)60528-8.
- Weiss JN, Korge P. . Circ. Res. 20 July 2001, 89 (2): 108–10. PMID 11463714. doi:10.1161/res.89.2.108.
- Srere PA. . Annu. Rev. Biochem. 1987, 56: 89–124. PMID 2441660. doi:10.1146/annurev.bi.56.070187.000513.
- Perham RN. . Annu. Rev. Biochem. 2000, 69: 961–1004. PMID 10966480. doi:10.1146/annurev.biochem.69.1.961.
- Huang X, Holden HM, Raushel FM. . Annu. Rev. Biochem. 2001, 70: 149–80. PMID 11395405. doi:10.1146/annurev.biochem.70.1.149.
- Mowbray J, Moses V. . Eur. J. Biochem. June 1976, 66 (1): 25–36. PMID 133800. doi:10.1111/j.1432-1033.1976.tb10421.x.
- Srivastava DK, Bernhard SA. . Science. November 1986, 234 (4780): 1081–6. PMID 3775377. doi:10.1126/science.3775377.
- Groll M, Clausen T. . Curr. Opin. Struct. Biol. December 2003, 13 (6): 665–73. PMID 14675543. doi:10.1016/j.sbi.2003.10.005.
- Nandi D, Tahiliani P, Kumar A, Chandu D. (PDF). J. Biosci. March 2006, 31 (1): 137–55 [2019-08-11]. PMID 16595883. doi:10.1007/BF02705243. (原始内容存档 (PDF)于2019-08-11).
- Bobik, T. A. (PDF). Microbe (Am Soc Microbiol). 2007, 2: 25–31. (原始内容 (PDF)存档于2008-08-02).
- Yeates TO, Kerfeld CA, Heinhorst S, Cannon GC, Shively JM. . Nat. Rev. Microbiol. August 2008, 6 (9): 681–691. PMID 18679172. doi:10.1038/nrmicro1913.
- Badger MR, Price GD. . J. Exp. Bot. February 2003, 54 (383): 609–22. PMID 12554704. doi:10.1093/jxb/erg076.
- Cate JH. . Methods. November 2001, 25 (3): 303–8 [2019-08-11]. PMID 11860284. doi:10.1006/meth.2001.1242. (原始内容存档于2019-08-11).
- Provance DW, McDowall A, Marko M, Luby-Phelps K. . J. Cell Sci. 1 October 1993, 106 (2): 565–77 [2019-08-11]. PMID 7980739. (原始内容存档于2020-03-26).
- Luby-Phelps K, Castle PE, Taylor DL, Lanni F. . Proc. Natl. Acad. Sci. U.S.A. July 1987, 84 (14): 4910–3. PMC 305216. PMID 3474634. doi:10.1073/pnas.84.14.4910.
- Luby-Phelps K. . J. Cell. Biochem. June 1993, 52 (2): 140–7. PMID 8366131. doi:10.1002/jcb.240520205.
- Kholodenko BN. . J. Exp. Biol. June 2003, 206 (Pt 12): 2073–82. PMID 12756289. doi:10.1242/jeb.00298.
- Pesaresi P, Schneider A, Kleine T, Leister D. . Curr. Opin. Plant Biol. December 2007, 10 (6): 600–6. PMID 17719262. doi:10.1016/j.pbi.2007.07.007.
- Winey M, Mamay CL, O'Toole ET. . J. Cell Biol. June 1995, 129 (6): 1601–15 [2019-08-11]. PMC 2291174. PMID 7790357. doi:10.1083/jcb.129.6.1601. (原始内容存档于2005-08-24).
- Weisiger RA. . Mol. Cell. Biochem. October 2002, 239 (1–2): 35–43. PMID 12479566. doi:10.1023/A:1020550405578.
- Maxfield FR, Mondal M. . Biochem. Soc. Trans. June 2006, 34 (Pt 3): 335–9. PMID 16709155. doi:10.1042/BST0340335.
- Pelham HR. . Philos. Trans. R. Soc. Lond. B Biol. Sci. August 1999, 354 (1388): 1471–8. PMC 1692657. PMID 10515003. doi:10.1098/rstb.1999.0491.
- Kamal A, Goldstein LS. . Curr. Opin. Cell Biol. February 2002, 14 (1): 63–8. PMID 11792546. doi:10.1016/S0955-0674(01)00295-2.
- Hoppert M, Mayer F. . Cell Biochem. Biophys. 1999, 31 (3): 247–84. PMID 10736750. doi:10.1007/BF02738242.
- Foster LJ, de Hoog CL, Zhang Y. . Cell. April 2006, 125 (1): 187–99. PMID 16615899. doi:10.1016/j.cell.2006.03.022.
- Herrgård, MJ; Swainston, N; Dobson, P; Dunn, WB; Arga, KY; Arvas, M; Blüthgen, N; Borger, S; Costenoble, R; 等. . Nature Biotechnology. October 2008, 26 (10): 1155–60. PMC 4018421. PMID 18846089. doi:10.1038/nbt1492.
- Stryer, Lubert; Berg, Jeremy Mark; Tymoczko, John L. . San Francisco: W.H. Freeman. 2002. ISBN 0-7167-4684-0. OCLC 179705944.
- Ohlrogge J, Pollard M, Bao X. . Biochem. Soc. Trans. December 2000, 28 (6): 567–73. PMID 11171129. doi:10.1042/BST0280567.
- Ohlrogge JB, Kuhn DN, Stumpf PK. . Proc. Natl. Acad. Sci. U.S.A. March 1979, 76 (3): 1194–8. PMC 383216. PMID 286305. doi:10.1073/pnas.76.3.1194.
- Goodman CD, McFadden GI. . Curr Drug Targets. January 2007, 8 (1): 15–30. PMID 17266528. doi:10.2174/138945007779315579.
延伸閱讀
- Wheatley, Denys N.; Pollack, Gerald H.; Cameron, Ivan L. . Berlin: Springer. 2006. ISBN 1-4020-4926-9. OCLC 71298997.
