苦味酸
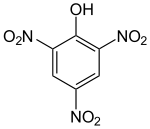
苦味酸,化学名2,4,6-三硝基苯酚,字母缩写TNP、PA,是一种炸药,名字由希腊语的πικρος(苦味)得来,味道很苦。纯淨物室温下呈略带黄色的结晶(黃色炸藥),难溶于四氯化碳,微溶于二硫化碳,易溶于丙酮、苯等有机溶剂,溶于热水、乙醇、乙醚。它是苯酚的三硝基取代物,受硝基吸电子效应的影响而有很强的酸性。
| 苦味酸 | |||
|---|---|---|---|
 | |||
| |||
| IUPAC名 2,4,6-Trinitrophenol | |||
| 别名 | 三硝基苯酚、2,4,6-三硝基苯酚、黃色炸藥 | ||
| 识别 | |||
| 缩写 | TNP、PA | ||
| CAS号 | 88-89-1 | ||
| ChemSpider | 6688 | ||
| SMILES |
| ||
| InChIKey | OXNIZHLAWKMVMX-UHFFFAOYAM | ||
| RTECS | TJ7875000 | ||
| DrugBank | DB03651 | ||
| 性质 | |||
| 化学式 | C6H3N3O7 | ||
| 摩尔质量 | 229.10 g·mol⁻¹ | ||
| 外观 | 无色至黄色针状结晶或大块固体 | ||
| 密度 | 1.763 g/cm³ (固) | ||
| 熔点 | 122.5 °C | ||
| 沸点 | > 300 °C(爆炸) | ||
| 溶解性(水) | 1.40 g/100 mL | ||
| pKa | 0.38 | ||
| 热力学 | |||
| ΔfHm |
-220 kJ·mol-1 | ||
| 危险性 | |||
| 警示术语 | R:R1, R10, R36, R37, R38 | ||
| 安全术语 | S:S28, S35, S37, S45 | ||
| NFPA 704 |
 4
3
4
| ||
| 爆炸性 | |||
| 撞击感度 | 24%-36% | ||
| 摩擦感度 | 0% | ||
| 爆速 | 7,350 m/s, ρ 1.70 | ||
| 相关物质 | |||
| 其他阳离子 | 苦味酸铵 | ||
| 相关化学品 | 三硝基甲苯 | ||
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |||
干燥的苦味酸感度较低,略高于TNT(三硝基甲苯),储存和运输都比较安全。但是某些苦味酸盐的感度较高,因此储存苦味酸必须用非金属容器,装于弹体中的苦味酸必须经过严格的干燥,以阻止苦味酸腐蚀金属,生成高感度的盐。
苦味酸的氧平衡为-45.39%,爆发点320℃(5s),当密度为1.70g·cm-3时,爆热和爆速分别为4.52MJ·kg-1和7.35km·s-1;密度为1.72g·cm-3时,爆压为26.5GPa,爆温约3000K,爆容约680L·kg-1。撞击感度24%-36%,对摩擦不敏感。做功能力为315cm3(铅孔扩张值),等效105%TNT当量;猛度16mm(铅柱压缩值),等效103%TNT当量。[1]
合成
直接硝化苯酚(即使是稀硝酸)也会造成高分子量的焦油形成,为了最小化这些副反应,苦味酸是通过苯酚的磺化制得苯酚二磺酸,再用浓硝酸硝化制得。该过程磺基被置换,先形成2,4-二硝基苯酚或2,6-二硝基苯酚,该反应过程高度放热,需仔细控制温度,否则会造成产率降低。随后再进一步硝化引入硝基,制得三硝基苯酚。
用途
苦味酸发明于公元1771年,在发明之后近一个世纪时间里,一直用作黄色染料。后因为爆炸事故,爆炸性质才被人们发现,成为世界上最早的合成炸药。基于它用做黄色染料的历史和极强的染黄色能力,又被称为黄色炸药,曾广泛用于装填炮弹、航空炸弹、地雷、手榴弹等几乎所有军用弹药。1873年,Hermann Sprengel发现苦味酸可以作为起爆药,并可用于军事高爆炸药。 1885年,法国化学家Eugène Turpin申请了专利,把苦味酸作为炸药与炮弹发射装药。全世界主要国家迅速发生了一场军事技术革命:1887年法国采用了苦味酸与火棉混合炸药,称为melinite(中译麦宁炸药);1888年英国开始制造类似的炸药,称为lyddite(中译立德炸药、裂地药、列底炮药);日本制造了改进的下濑火药;1889年,奥匈帝国开始制造了苦味酸与三硝基甲酚胺盐混合的炸药ecrasite;1894年,沙俄开始把苦味酸用作炮弹发射药;1906年,美国使用苦味酸胺(称作Dunnite或explosive D)。
中日甲午戰爭、1898年英国殖民苏丹的恩图曼战役、布尔战争、日俄战争、第一次世界大战,都广泛使用了苦味酸炸药。
由于苦味酸容易与弹体金属反应,产生感度很高的苦味酸盐,所以时常发生弹药的意外爆炸,造成士兵伤亡。1917年12月6日加拿大的哈利法克斯大爆炸造成了2000余人死亡,就是由于苦味酸炮弹的安全事故造成的。1943年陆奥号战列舰爆炸也被怀疑与之相关。1902年,德国开始用更稳定、安全的TNT替代苦味酸作为炮弹装药。第一次世界大战中世界其它各国陆续完成替换苦味酸军用炸药。在20世纪下半叶趋于淘汰。苦味酸也是重要的化工原料,酸碱指示剂和医用收敛药。
参考资料
- 欧育湘等. . 北京理工大学出版社. 2006年1月: 178. ISBN 7-5640-0475-4.
- Cooper, Paul W., Explosives Engineering, New York: Wiley-VCH, 1996. ISBN 0-471-18636-8


