硝酸
硝酸(分子式:HNO3)是一种强酸,是三酸兩鹼其一,其水溶液俗称硝镪水。纯硝酸为无色液体,沸点83℃,味苦,在-42℃时凝结为无色晶体,与水混溶,有强氧化性和腐蚀性。其不同浓度水溶液性质有别,市售浓硝酸为共沸物,溶质质量分数为69.2%,一大气压下沸点为121.6℃,密度为1.42g·cm-3,约16mol·L-1,溶质重量百分比足够大(市售浓度最高为98%以上)的,称为发烟硝酸,硝酸是一种重要的化工原料。
| 硝酸 | |
|---|---|
 | |
 | |
 | |
| IUPAC名 Nitric acid | |
| 别名 | 硝镪水 |
| 识别 | |
| CAS号 | 7697-37-2 |
| PubChem | 944 |
| ChemSpider | 919 |
| SMILES |
|
| InChI |
|
| InChIKey | GRYLNZFGIOXLOG-UHFFFAOYAO |
| Gmelin | 1576 |
| 3DMet | B00068 |
| UN编号 | 2031 |
| EINECS | 231-714-2 |
| ChEBI | 48107 |
| RTECS | QU5775000 |
| KEGG | D02313 |
| MeSH | Nitric+acid |
| 性质 | |
| 化学式 | HNO3 |
| 摩尔质量 | 63.012 g·mol⁻¹ |
| 外观 | 无色清澈液体 |
| 密度 | 1.51 g/cm³ |
| 熔点 | -42 °C(231 K) |
| 沸点 | 83 °C(356 K)(纯酸) (68%aq沸点120.5℃) |
| 溶解性(水) | 完全混溶 |
| 偶极矩 | 2.17±0.02D |
| 危险性 | |
欧盟危险性符号 氧化性 O 氧化性 O 腐蚀性 C 腐蚀性 C | |
| 警示术语 | R:R8-R35 |
| 安全术语 | S:S1/2-S23-S26-S36-S45 |
| NFPA 704 |
 0
4
0
OX
|
| 闪点 | 不可燃 |
| 相关物质 | |
| 相关化学品 | 亚硝酸 五氧化二氮 |
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |
歷史
硝酸和硫酸一样由公元8世纪阿拉伯鍊金術士阿布·穆薩·賈比爾·伊本·哈揚(Jabir ibn Hayyan)在乾餾綠矾和硝石混合物時發現,也是一種化學肥料。[1]因為硝酸是在硝石中發現的,所以含氧氮酸不叫氮酸,叫硝酸。
自然存在
雷雨时能产生少量的硝酸。打雷時放出的能量讓空氣中的N2和O2發生反應,產生NO:
- N2 + O2 → 2NO
- 2NO + O2 → 2NO2
- N2 + 2O2 → 2NO2
NO2和水反應產生硝酸和一氧化氮:
- 3NO2 + H2O → 2HNO3 + NO
结构
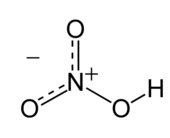
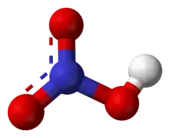
硝酸是平面分子,其中心原子N原子为sp2杂化。由于羟基上的氢原子与另外一个氧原子形成了氢键,分子才呈平面结构,而且N的三根键长都不相同。N原子垂直于分子平面的一个p轨道是满的,它与未连接H的两个氧原子上的p轨道共轭,形成大Π键。分子内氢键也是硝酸沸点较低的原因。
硝酸去掉一个氢原子的结构是硝酸根,一般带一个负电荷(硝酸根离子)。硝酸根具有对称的平面等边三角形结构,4个原子形成大键,多出来的1个电子在离域Π键裡。
物理性质
純硝酸為無色、容易揮發的液體,沸點約為83℃,凝固点约为-42℃,密度为1.51g/ml。可以与水以任意比混溶。硝酸是二氧化氮溶於水生成的,但由於二氧化氮溶於水並不會完全水解成硝酸,會有少量的二氧化氮分子存在,因此硝酸水溶液呈淡黃色,也会挥发出棕红色的NO2。一般的浓硝酸指的是16mol/L的HNO3水溶液,密度为1.42g/ml。
 發煙硝酸
發煙硝酸 70%硝酸
70%硝酸
化学性质
纯硝酸可以发生自偶电离:2HNO3⇌H2O+NO2++NO3-
硝酸作为氮的最高价(+5)水化物,具有很强的酸性,一般情况下认为硝酸的水溶液是完全电离的。硝酸可以与醇发生酯化反应,如硝酸甘油的制备。(實際上我們會使用浓硫酸,产生大量NO2+),成本較低而且較容易處理,與其他更強的脫水劑,例如P4O10,也可以產生大量的硝醯陽離子,这是硝化反应能进行的本质。
- HNO3 + H2O → H3O+ + NO3- (水中)
- HO-NO2 + 2H2SO4 → NO2+ + 2HSO4- + H3O+ (浓硫酸中)
硝酸的水溶液无论浓稀均具强氧化性及腐蚀性,溶液越浓其氧化性越强。硝酸在光照条件下分解成水、NO2和O2,方程式如下:
- 4HNO3 → 4NO2 + O2 + 2H2O
因此硝酸一定要盛放在棕色瓶中,並置於阴凉处保存。硝酸能溶解许多种金属(例如银),生成盐、水、氮氧化物。随着溶液浓度的减小,其还原产物逐渐由高价向低价过渡,从最浓到最稀可生成NO2、NO、N2O、N2、NH4NO3。还原产物一般是混合物,金属与濃硝酸反应多生成NO2,與稀硝酸反應下生成如NO等較低價化合物。
铁、铝、铬等金属遇冷的浓硝酸可以发生钝化现象,只在表面形成一层致密的氧化膜,不会完全反应掉。
浓硝酸和浓盐酸的物質的量按1:3混合,即为王水,能溶解金、铂等稳定金属。
硝酸盐大多易遇热分解,生成氧气、氮氧化物、金属氧化物(也可能生成亚硝酸盐等)。
硝酸铵中的硝酸根與銨根,平均能量大於有其平均價數之一氧化二氮,在固態時發生均化反應(因為動力學原因,在溶液內不發生)(NH4NO3)即加热或撞击分解生成一氧化二氮和水,一般使用現代合成炸藥引爆,威力與TNT相去不遠,但成本極低。因此被用于国防工业及工程上而被譽為國防工業之母(主要製造硝基含能化合物(現代合成炸藥)。硝酸钾就是黑火药的成分之一)。
由於硝酸也屬於強酸,所以可以和鹼發生酸鹼中和反應。
HNO3+NaOH→NaNO3+H2O
制备
4NH3(g)+5O2(g)→4NO(g)+6H2O(g)(鉑銠催化)(ΔH=−905.2kJ)
2NO(g)+O2(g)→2NO2(g) (ΔH=−114kJ/mol)
3NO2(g)+H2O(l)→2HNO3(aq)+NO(g) (ΔH=−117kJ/mol)
工业用途
硝酸是在工业上和实验室中都很常用的一种酸。
作为硝酸盐和硝酸酯的必需原料,硝酸被用来制取一系列硝酸盐类氮肥,如硝酸铵、硝酸钾等;也用来制取硝酸酯类或含硝基的炸药,如三硝基甲苯(TNT)、硝化甘油。
人体影响
硝酸不论浓稀溶液都有氧化性和腐蚀性,因此对人很危险,仅溅到皮肤上也会引起严重烧伤。皮肤接触硝酸后会慢慢变黄,最后变黄的表皮会起皮脱落(硝酸和蛋白質接觸後,會導致黄蛋白反应而變性)。此外,濃硝酸需以深色玻璃瓶盛裝,避免受到光照反應釋出有毒的NO2。
与金属的反应
- 2HCl(aq) + Zn(s) → ZnCl2(aq) + H2(g)
而硝酸与金属反应,不会生成氢气。这是因为硝酸根(NO3-)的氧化性比氢离子(H+)强。
浓硝酸(约16mol/L)与金属反应,主要生成红棕色的二氧化氮气体:
- Zn(s) + 4HNO3(aq) → Zn(NO3)2(aq) + 2NO2(g) + 2H2O(l)
稀硝酸(约6mol/L)与金属反应,主要生成一氧化氮气体:
- 3Zn(s) + 8HNO3(aq) → 3Zn(NO3)2(aq) + 2NO(g) + 4H2O(l)
更稀的硝酸(约2mol/L以下)与金属反应,产物从一氧化二氮到氮气到铵根离子不等。
普遍认为,硝酸与金属反应时,各还原产物(NO2、NO、N2O、N2、NH3)都可以生成。 但由于硝酸、水、氮氧化物、亚硝酸、连二次硝酸等物质间的多个平衡,不同浓度硝酸的还原产物有很大差异。
极稀硝酸和活泼金属生成氢气的说法,没有得到证实。
注释
- . [2020-09-15]. (原始内容存档于2010-01-29).
- P. W. Atkins, Molecules, 1987, ISBN 0-7167-5019-8
