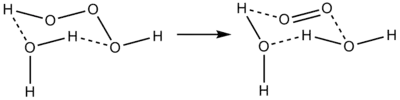过三氧化氢
过三氧化氢也称为“三氧化氢”或“三氧化二氢”,其化学式为“H2O3”或“HOOOH”,是氢元素的氧化物。他是一种不稳定的化合物,在水溶液中会分解为水和单线态氧:
| 过三氧化氢 | |
|---|---|
| IUPAC名 Trioxidane 三氧烷 | |
| 别名 | Dihydrogen trioxide |
| 识别 | |
| CAS号 | 14699-99-1 |
| PubChem | 166717 |
| ChemSpider | 145859 |
| SMILES |
|
| InChI |
|
| InChIKey | JSPLKZUTYZBBKA-UHFFFAOYAV |
| Gmelin | 200290 |
| ChEBI | 46736 |
| 性质 | |
| 化学式 | H2O3 |
| 摩尔质量 | 50.01 g·mol−1 |
| 精确质量 | 50.000393930 g mol-1 |
| 外观 | 无色至微紫色液体 |
| 密度 | 1.672 g/cm3 |
| 溶解性(水) | 与水混溶 |
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |
上述反应的逆反应(向水分子中插入单线态氧原子)一般情况下由于单线态氧原子不足而速率小于正反应速率。
理论研究表明,过三氧化氢有顺式和反式共两种异构体,其中反式异构体比顺式异构体更稳定。二阶全活化空间微扰理论(complete active space perturbation theory of second order,CASPT2)预测结果显示,在单激发态中,顺式过三氧化氢寿命最长的激发态为21A",跃迁能为167.43nm,寿命为1.44×10-5s;而反式过三氧化氢寿命最长的激发态为21A,其跃迁能为165.52nm,寿命为2.07×10-5s。[1]
制备
过三氧化氢可由O3和H2O2的反应或水的电解少量制备。用以上两种反应制得的过H2O3的量虽然较少,但已可检测出其存在。
若需获得大量H2O3,则要利用有机还原剂(例如氢化偶氮苯)在有机溶剂中低温还原O3,H2O3也能在有机过三氧化氢分解时产生(ROOOH)。[3]
结构
光谱学分析已指出H2O3分子具有曲折的结构(H-O-O-O-H),具有C2对称性,其中,H2O3O-O键的键长约为142.8pm,略短于H2O3中的146.4pm。O-H键的键长为96.6pm,H-O-O键角为101.9°,O-O-O键角为106.8°,H-O-O-O二面角为81.2°。[3]
存在与存在形式
由于在生命系统中H2O3像臭氧/过氧化氢混合物一样,也能由人体内的抗体能产生,并利用其强氧化性对抗入侵的细菌等病原体。所以新近的研究认为H2O3是上述混合物中起抗菌作用的活性物质。[2][6]生命系统中H2O3由免疫细胞产生的单线态氧和水反应获得(该化学反应的方向视各物质的浓度而定)。[3][7]
2005年,H2O3被利用微波光谱学在超音速客机中发现,其分子呈现反式构象(trans conformation),其中的O-O键短于H2O2中的O-O键。
计算化学方面的预测表明还可能有包含更多氧原子的链状分子(或多氧化氢)存在,在低温气体中,甚至连具有无数个氧原子的链也可能存在。
参考文献
- 王连宾、吴文鹏、张敬来. . 物理化学学报. 2006, 22 (8): 1079–1084.
- Paul T. Nyffeler, Nicholas A. Boyle, Laxman Eltepu, Chi-Huey Wong, Albert Eschenmoser, Richard A. Lerner, Paul Wentworth Jr. . Angewandte Chemie International Edition. 2004, 43 (35): 4656–4659. PMID 15317003. doi:10.1002/anie.200460457.
- Božo Plesničar. . Acta Chim. Slov. 2005, 52: 1–12.
- Xin Xu and William A. Goddard III. .
- Kohsuke Suma, Yoshihiro Sumiyoshi, and Yasuki Endo. . J. Am. Chem. Soc. 2005, 127 (43): 14998–14999 [2020-09-19]. PMID 16248618. doi:10.1021/ja0556530. (原始内容存档于2013-05-23).
- A Time-Honored Chemical Reaction Generates an Unexpected Product, News & Views, September 13, 2004
- Roald Hoffmann. . American Scientist. 2004.