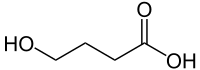
γ-羟基丁酸
-羟基丁酸,又称4-羟基丁酸,(,),是一种在中枢神经系统中发现的天然物质,亦存在于葡萄酒、牛肉、柑橘属水果中,也少量存在于几乎所有动物体内[1]。该神经药物因无色无味並会導致暂时性记忆丧失、噁心、呕吐等症状,而被犯罪分子用作麻醉药品或迷姦药物,中文又稱神仙水、聽話水,或迷姦水。
 | |
 | |
| 系统(IUPAC)命名名称 | |
|---|---|
4-Hydroxybutanoic acid | |
| 临床数据 | |
| 妊娠分级 |
|
| 给药途径 | 口服、静脉注射 |
| 合法狀態 | |
| 合法状态 |
|
| 药代动力学数据 | |
| 生物利用度 | 25% (口服) |
| 代谢 | 95%,主要为肝脏代谢,其次为血液和组织 |
| 生物半衰期 | 30–60分钟 |
| 排泄 | 5% (肾脏) |
| 识别 | |
| CAS注册号 | 591-81-1 |
| ATC代码 | N01AX11 |
| PubChem | CID 3037032 |
| DrugBank | DB01440 |
| ChemSpider | 9984 |
| 其他名称 | GHB |
| 化学 | |
| 化学式 | C4H8O3 |
| 摩尔质量 | 104.10 g/mol (-羟基丁酸) 126.09 g/mol (钠盐) 142.19 g/mol (钾盐) |
| |
-羟基丁酸可在人体细胞内合成,结构上与酮体β-羟基丁酸相似。在实际使用中,通常使用-羟基丁酸的钾盐或钠盐。-羟基丁酸也可由发酵产生,因此也存在于一些啤酒或葡萄酒中。琥珀酸半醛脱氢酶缺乏症可造成GHB在血液中累积,造成麻醉效果。
历史上,-羟基丁酸曾被用作常用镇静剂,用于治疗失眠、抑郁症、发作性嗜睡病和酗酒,也被用于提高运动员成绩[2]。它在美国属于限制使用药物,被称作Xyrem,由Jazz Pharmaceuticals公司销售[3],用于治疗与发作性嗜睡病患者的日间嗜睡症状。该神经药物在许多地区被认定为毒品而禁用[4](其在中国大陆是第一类精神药品,在台湾是管制类精神药物[5][6])。
历史
4-羟基丁酸由俄國化學家亚历山大·扎伊采夫于1874年首次合成。[7]1960年代初,法國神經生物學家Henri Laborit博士在研究神经递质γ-氨基丁酸(GABA)时对4-羟基丁酸对人的作用进行了全面研究[8]。4-羟基丁酸很快被大量使用,因为它副作用小,持续时间短。但其缺点是应用剂量范围窄(虽然有很高的半数致死量),且当与酒精或其他中枢神经系统镇静剂混用时会有危险。
在法国、意大利和其他欧洲国家,-羟基丁酸几十年来一直被大量使用,作为安眠药和分娩时的麻醉剂。但其被滥用的问题和新药的开发已导致4-羟基丁酸的使用日益减少。现在-羟基丁酸一般只被用于治疗嗜睡症,同时也越来越少地被用于酗酒的治疗。
性质及制备
-羟基丁酸熔点202℃,沸点193-197℃(747 torr),密度1.1405g·cm-3,pKa为4.67,本征溶解度为51.2g(25℃)。[9]
一般-羟基丁酸由向γ-丁内酯(GBL)的乙醇或水溶液中加入氢氧化钠(碱液)的方法合成。但是由于原料γ-丁内酯被限制使用,现在开始更多地采用以四氢呋喃(THF)为原料进行合成。
药理学
在中枢神经系统中,4-羟基丁酸至少有两个特异性结合位点[10]。-羟基丁酸可作用于新发现的-羟基丁酸受体产生兴奋[11][12],也可作用于γ-氨基丁酸受体产生抑制[12]。-羟基丁酸可在哺乳动物大脑()内自然合成,并发挥神经递质的作用[13]。-羟基丁酸可在γ-氨基丁酸神经元中由γ-氨基丁酸合成,并在神经元兴奋时释放出去[12]。
医疗用途
-羟基丁酸自1960年代[2]开始被用作常用麻醉剂,治疗失眠、抑郁症并用于提高运动成绩。在意大利,-羟基丁酸以Alcove的商品名(ATC代码N07BB)出售,γ-羟丁酸被用于治疗酒精依赖(每天50至100毫克每公斤体重,分3次或更多次服用),包括迅速戒酒和短期到长期戒毒。
参考文献
- Weil A, Rosen W. l 请检查
|url=值 (帮助). 2nd. Boston/New York: Houghton Mifflin Company. 1993: 77. ISBN 978-0-395-66079-9. 已忽略未知参数|chapter-url-access=(帮助) - Theodore I Benzer. . eMedicine. January 8, 2007.
- . [2009-07-07]. (原始内容存档于2008-05-22).
- Erowid GHB Vault : Legal Status
- 警籲勿碰新興毒品神仙水
- . [2018-11-11]. (原始内容存档于2018-11-11).
- Alexander Saytzeff. . Liebigs Annalen der Chemie. 1874, 171: 258–290. doi:10.1002/jlac.18741710216.
- H. Laborit, J.M. Jouany, J. Gerald, F. Fabiani. . Aggressologie. 1960, 1: 407.
- Retrieved from SciFinder. [2018-1-11]
- Wu Y, Ali S, Ahmadian G; 等. . Neuropharmacology. December 2004, 47 (8): 1146–56. PMID 15567424. doi:10.1016/j.neuropharm.2004.08.019.
- Cash, C. . Biochemical Pharmacology. 1999, 58: 1815. doi:10.1016/S0006-2952(99)00265-8.
- Maitre M, Humbert JP, Kemmel V, Aunis D, Andriamampandry C. . Med Sci (Paris). March 2005, 21 (3): 284–9 [2009-07-11]. PMID 15745703. (原始内容存档于2009-07-15) (法语).
- Waszkielewicz A, Bojarski J. (PDF). . 2004, 56 (1): 43–9. PMID 15047976.
外部链接
- 认知增强研究所 - 对GHB与其它物质的研究发现
- EMCDDA关于GHB与新合成药混用的风险评估报告
- Erowid数据库中有关GHB的内容 页面存档备份,存于
- 苯二氮和GHB (国家药物滥用研究所)
- Pubmed/关于羟基丁酸钠与酗酒的医药学研究
