碘苯
| 碘苯 | |||
|---|---|---|---|
| |||
| IUPAC名 Iodobenzene | |||
| 别名 | 碘代苯 | ||
| 识别 | |||
| CAS号 | 591-50-4 | ||
| PubChem | 11575 | ||
| ChemSpider | 11087 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | SNHMUERNLJLMHN-UHFFFAOYAQ | ||
| RTECS | DA3390000 | ||
| DrugBank | DB02252 | ||
| 性质 | |||
| 化学式 | C6H5I | ||
| 摩尔质量 | 204.01 g·mol⁻¹ | ||
| 外观 | 对光敏感的无色液体 | ||
| 密度 | 1.831 g/cm3(20/4℃) | ||
| 熔点 | -29 ℃ | ||
| 沸点 | 188 ℃(常压)63-64 ℃(1.07kPa) | ||
| 折光度n D |
1.6200(18.5℃) | ||
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |||
性质
碘苯是无色有特殊气味的液体,难溶于水,可溶于氯仿、乙醚和乙醇。对光敏感,见光颜色逐渐变黄。闪点74℃。
由于 C-I 键键能比 C-Cl 和 C-Br 键键能低,因此碘苯的反应性比氯苯和溴苯更强。它可以与镁反应生成格氏试剂苯基碘化镁(PhMgI),后者可在有机合成中用作苯基负离子的合成子等价物。
制备
由苯胺重氮化、置换制得。首先向冷却的苯胺盐酸溶液中缓慢滴加亚硝酸钠溶液,并用碘化钾淀粉试纸测定反应终点(蓝色),使之发生重氮化反应生成重氮盐PhN2+Cl−,然后加入碘化钾溶液,使重氮基被碘取代并放出氮气,生成碘苯。反应后加入强碱使过量的亚硝酸盐水解,酸化,最后用水蒸汽蒸馏收集产物,即得到纯净的碘苯。[1]
除上述方法外,碘苯也可通过用碘、硝酸和苯在回流条件下反应得到。[2]
还有一种制取碘苯和取代碘苯的方法是:先用三氧化二铊与含水三氟乙酸加热反应制取三氟乙酸铊,然后在存在三氟乙酸的情况下加入苯反应,生成二(三氟乙酸)苯基铊,最后将二(三氟乙酸)苯基铊与碘化钾水溶液反应,便可得到碘苯,产率高达96%。
2-碘对二甲苯用上述铊法制取的过程可总结为:
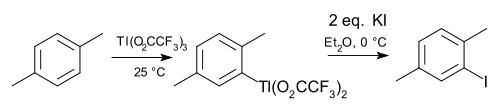
2-碘对二甲苯的制取
参考资料
- H. J. Lucas, E. R. Kennedy (1939). "Iodobenzene". Org. Synth.; Coll. Vol. 2: 351.
- F. B. Dains and R. Q. Brewster (1941). "Iodobenzene". Org. Synth.; Coll. Vol. 1: 323.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.