甘草酸
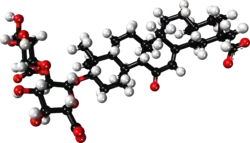
甘草酸(Glycyrrhizin,或glycyrrhizic acid,glycyrrhizinic acid)是甘草(Glycyrrhiza glabra)根的主要甜味成分。在结构上是一种皂苷。可用作食品和化妆品中的乳化剂和凝胶形成剂。其糖苷配基是甘草次酸,在日本被用于降低慢性丙型肝炎患者患肝癌的风险的前体药物。[3] [4]
 | |
 | |
| 系统(IUPAC)命名名称 | |
|---|---|
(3β,20β)-20-carboxy-11-oxo-30-norolean-12-en-3-yl 2-O-β-D-glucopyranuronosyl-α-D-glucopyranosiduronic acid OR (1R,2S,5S,8S,10R,14R,15S,18S,20R)-18-{[(2S,3R,4S,5S,6S)-6-carboxy-3-{[(2R,3R,4S,5S,6S)-6-carboxy-3,4,5-trihydroxyoxan-2-yl]oxy}-4,5-dihydroxyoxan-2-yl]oxy}-1,2,5,8,15,19,19-heptamethyl-13-oxopentacyclo[12.8.0.02,11.05,10.015,20]docos-11-ene-8-carboxylic acid | |
| 临床数据 | |
| 商品名 | Epigen, Glycyron |
| Drugs.com | 国际药品名称 |
| 给药途径 | 口服、静脉注射 |
| 药代动力学数据 | |
| 代谢 | 肝脏和肠道细菌 |
| 生物半衰期 | 6.2-10.2 h[1] |
| 排泄 | 粪便、尿液 (0.31-0.67%)[2] |
| 识别 | |
| CAS注册号 | 103000-77-7(β-D-Glucopyranosiduronic acid) 1405-86-3(α-D-Glucopyranosiduronic acid) |
| ATC代码 | A05BA08 QA05BA08 (vet) |
| PubChem | CID 128229 |
| ChemSpider | 14263 |
| UNII | 6FO62043WK |
| ChEBI | CHEBI:15939 |
| ChEMBL | CHEMBL441687 |
| 化学 | |
| 化学式 | C42H62O16 |
| 摩尔质量 | 822.93 g/mol |
| |
| |
| 物理性质 | |
| 水溶液 | 1-10 mg/mL (20 °C) |
不良影响
通过食用黑甘草使用甘草酸的最广泛报道的副作用是降低血钾水平,对体液平衡和神经功能有影响。[5] [6] 长期服用黑甘草,即使是适量,也会导致血压升高, [6]可能导致心律不齐 ,以及与处方药的不良反应。 [5]
其对体液的影响与肾脏内皮质醇代谢的抑制,和随后对盐皮质激素受体的刺激, [7]以及血液中肾素、钾和醛固酮的水平降低有关,这些因素共同导致血压升高。 [6]
药代动力学
口服摄入后,甘草酸首先被肠道细菌水解为18β-甘草次酸(Enoxolone)。 从肠道完全吸收后,18β-甘草次酸被代谢成肝脏中的3β-单葡糖醛酸-18β-甘草次酸。然后该代谢物在血流中循环。主要部分被胆汁清除,只有一小部分(0.31-0.67%)被尿液清除。 [9] 口服摄入600mg甘草酸后,1.5至14小时后尿液中出现代谢物。1.5至39小时后达到最大浓度(0.49至2.69mg / l),并且在2至4天后仍可在尿液中检测到代谢物。[9]
调味特性
甘草酸是甘草根浸提后,在水中煮沸而得的提取物。[10] 甘草提取物(甘草酸)在美国作为液体、糊剂或喷雾干燥粉末出售。 [10] 当在规定量范围时,它被批准用作制造食品,饮料,糖果, 膳食补充剂和调味品中的香料和香味剂 。 [10]它的甜度是蔗糖(食糖)的30至50倍。 [8] [11]
参考文献
- van Rossum, TG; Vulto, AG; Hop, WC; Schalm, SW. . Clinical Therapeutics. December 1999, 21 (12): 2080–90. PMID 10645755. doi:10.1016/S0149-2918(00)87239-2. hdl:1765/73160.
- Ploeger, B; Mensinga, T; Sips, A; Seinen, W; Meulenbelt, J; DeJongh, J. . Drug Metabolism Reviews. May 2001, 33 (2): 125–47. PMID 11495500. doi:10.1081/DMR-100104400.
- Arase, Yasuji; Ikeda, Kenji; Murashima, Naoya; Chayama, Kazuaki; Tsubota, Akihito; Koida, Isao; Suzuki, Yoshiyuki; Saitoh, Satoshi; Kobayashi, Masahiro. . Cancer. 15 April 1997, 79 (8): 1494–1500. doi:10.1002/(SICI)1097-0142(19970415)79:8<1494::AID-CNCR8>3.0.CO;2-B.
- Fiore, C; Eisenhut, M; Krausse, R; Ragazzi, E; Pellati, D; Armanini, D; Bielenberg, J. . Phytotherapy Research. 2008, 22 (2): 141–8. PMID 17886224. doi:10.1002/ptr.2295.
- . US Food and Drug Administration. 30 October 2017 [15 December 2017].
- Penninkilampi, R; Eslick, E. M; Eslick, G. D. . Journal of Human Hypertension. 2017, 31 (11): 699–707. PMID 28660884. doi:10.1038/jhh.2017.45.
- Ferrari, P.; Sansonnens, A.; Dick, B.; Frey, F. J. . Hypertension. 2001, 38 (6): 1330–6. PMID 11751713. doi:10.1161/hy1101.096112.
- Asl, MN; Hosseinzadeh, H. . Phytotherapy Research. 1 June 2008, 22 (6): 709–24. PMID 18446848. doi:10.1002/ptr.2362.
- Kočevar Glavač, Nina; Kreft, Samo. . Food Chemistry. 2012, 131: 305–308. doi:10.1016/j.foodchem.2011.08.081.
- . US Food and Drug Administration, Code of Federal Regulations Title 21, 21CFR184.1408. 1 April 2017 [15 December 2017].
- . PubChem. National Institutes of Health. [24 February 2014].
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
