维生素E
維他命E(英語:)是一組八種的脂溶性維他命[1],包括了四種生育酚及另外四種生育三烯酚[2]。它是最主要的抗氧化劑之一,它不溶於水,卻可溶於脂肪和乙醇等有機溶劑中,於油炸時其活性會明顯降低;對熱力和酸性穩定,對鹼性不穩定;對氧氣敏感,但對熱力不敏感。維他命E缺乏症很罕見,這通常是由於消化膳食脂肪的潛在問題而非飲食中缺乏維他命E所引起的[3],而缺乏維他命E會引致神經系統疾病[4]。維他命E也是一種脂溶性抗氧化劑,可保護細胞膜免受活性氧類的侵害[1][4]。
| 维生素E | |
|---|---|
| 药物种类 | |
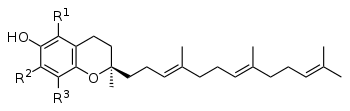
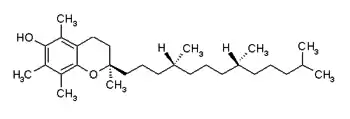 維他命E的RRR-α-生育酚形式。 | |
| 用途 | 維他命E缺乏症 抗氧化劑 |
| 生物目标 | 活性氧類 |
| ATC代码 | A11HA03 |
| 外部链接 | |
| MeSH | D014810 |
| AHFS/Drugs.com | MedFacts天然产品 |
在世界上,各國政府組織建議成年人每天攝入7-15毫克範圍內的維他命E。截至2016年,根據全球100多項研究的總結,維他命E的攝入量都低於建議水平,該研究報告的α-生育酚的平均飲食攝入量為每天6.2毫克[5]。以α-生育酚為營養補充劑進行研究顯示,每天的劑量高達每天2,000mg的結果好壞參半[6]。人口研究表明,食用富含維他命E的食物或自行選擇服用維他命E的營養補充劑的人裡,心血管疾病、癌症、認知障礙症和其他疾病的發生率較低,但在安慰劑對照的臨床測試不能總是得出同樣的發現[1],並且有跡象表明維他命E的補充(每天≥400IU且維持至少一年)實際上跟死亡率所有成因的適度增加有關[7]。截至2017年,維他命E仍然是活躍的臨床研究主題[8]。這裡尚未有循證醫學證據表明於護膚品中使用維他命E是有效的[9]。天然和合成的生育酚都會被氧化,因此在膳食補充劑中會被酯化,產生生育酚乙酸酯以達到其穩定的目的[1][10]。
生育酚和生育三烯酚都以α(阿爾法)、β(貝塔)、γ(伽瑪)和 δ(德爾塔)的形式存在,這取決於苯甲醇環上甲基的數量和位置來決定[4][11]。所有這些維他命中的全部八種均具有色原烷雙環,並帶有氫原子以減少自由基的羥基和疏水性的側鏈,讓它可滲透到生物膜中。在多種不同形式的維他命E中,γ-生育酚是最常見於北美飲食的形式,但是α-生育酚具有最強的生物活性[1][12]。棕櫚油是生育三烯酚的來源。
維他命E於1922年被發現,在1935年分離出來並於1938年首次合成。由於首先確定了其維他命活性最初被認為是對於大鼠中的受精卵導致活產來說是必不可少的,因此它被命名為「生育酚(tocopherol)」,此名稱源自希臘語,意思為「出生」、「承受」和「攜帶」[13][14][15]。天然從植物油中提取的α-生育酚,或最常見的是合成生育酚乙酸酯,是以一種流行的膳食補充劑出售,它既可以單獨使用,也可以摻入綜合維他命產品中使用,也可以摻入油或乳液中用於皮膚上[1][9]。
在缺乏维生素E后进行补充,能促進性激素分泌,使男子精子活力和數量增加;使女子雌性激素濃度增高,提高生育能力,預防流產。 近来还发现维生素E可抑制眼睛晶状体内的过氧化脂反应,使末梢血管扩张,改善血液循环。维生素E苯环上的酚羟基被乙酰化, 酯水解为酚羟基后为生育酚。人们常误认为维生素E就是生育酚。
功能
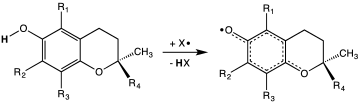
作為維他命,維他命E可能具有多種作用[4]。許多生物學功能已經被假定,包括作為脂溶性抗氧化劑的作用[4]。在這種作用下,維他命E充當著自由基清除劑,把氫原子(H)傳遞給自由基。在323kJ/mol時,生育酚的O—H鍵比其他大部分的苯酚弱了約10%[16]。這種薄弱的鍵使維他命能夠向超氧化氫及其他自由基貢獻氫原子,從而將其破壞作用降至最低。在透過氧化還原反應將由此產生的生育酚基團再循環至生育酚,如維他命C[17]。由於維他命E是脂溶性的,因此它可摻入到細胞膜中,從而保護細胞免受氧化的損害。
維他命E可影響基因表達[18],那是一種酶活性調節劑,例如是蛋白激酶C(PKC),它在平滑肌的生長中發揮作用 — 維他命E參與了PKC失活以抑制平滑肌的生長[19]。
維他命E的功能:
- 維他命E有助防止多元不飽和脂肪酸及磷脂質被氧化,故可維持細胞膜的完整性,並可保護維他命A不受氧化破壞,並一再加強其作用;
- 維他命E可與碘結合為化合物,已證實能預防維他命E缺乏症相關症狀的發生;
- 維他命E有防止血小板過度凝集的作用,並增進紅血球膜的安定及紅血球的合成;
- 維他命E可減少因空氣污染引起的效應,繼而使肺部的傷害降低;
- 維他命E可維持細胞的呼吸,減少老人斑的沉積對神經系統和骨骼肌具有保護作用;
一些研究報告顯示維他命E與防癌、抗老化有關,不過未得到廣泛證實。人體神經肌肉系統的正常發育和視網膜的功能需要充足的維他命E。神經系統在產生神經遞質的過程中,伴隨大量自由基的產生,因此在製造線粒體和神經系統的軸突膜受自由基損傷方面是必須使用到維他命E。適當攝入維他命E將有助於精子活力和整個精子健康,長期服用可以提高男性的性慾水平[20]。
攝取不足
維他命E缺乏症在人類中很罕見,那是由於飲食中脂肪吸收或代謝異常所致,並非由於維他命E含量低的飲食形成[3]。代謝遺傳異常的一個例子是α-生育酚轉移蛋白(α-TTP)編碼的基因突變。具有這種遺傳缺陷的人儘管攝入了正常分量的維他命E,他們都會表現出漸進式神經退行性疾病,稱為「維他命E缺乏症的共濟失調(AVED)」。他們需要大量的α-生育酚作為膳食補充劑以彌補α-TTP的缺乏[21][22]。由於吸收不良或代謝異常引起的維他命E缺乏症會引致神經系統疾病,這可能由於髓磷脂的結構和功能改變,導致沿著神經的電脈衝傳導不良所致。除了共濟失調外,維他命E缺乏症還會引起周邊神經病變、肌病、視網膜病變和免疫反應受損[3][4]。
其他由於缺乏維他命E引起的問題:
- 溶血性貧血 — 因為通過胎盤輸送給新生兒的維他命E很少,所以新生兒或早產兒的血漿中維他命E會偏低。若母體缺乏維他命E,導致幼兒維他命E不足時會引致幼兒血球容易破裂而發生貧血,稱為溶血性貧血,有時還會間接引發黃膽;
- 腸胃不適、陽痿、水腫、皮膚病害、肌肉衰弱;
- 慢性脂肪吸收不良;
- 溶血、肌尿酸、平滑肌中褐色素沉澱;
- 膀胱纖維症、血小板增多、掉髮、頭髮乾燥;
- 成年人缺乏維他命E多年後,會顯現紅血球的溶解增加;
- 月經失調、末稍血液循環障礙所致的手腳虛冷、凍傷等;
- 冷感症;
動物患病:
- 全脂肪織炎(黃色脂肪症、黃膘病):不飽和脂肪酸攝入過量會引起維他命E缺乏。
測試水平
全球約100多項人類研究的摘要報告指,血清裡α-生育酚的中位數為22.1µmol/L,並將α-生育酚缺乏症定義為<12 µmol/L。它引用了一項建議,即血清α-生育酚濃度應≥30 µmol/L,以改善健康[5]。相反,美國關於維他命E的飲食參考攝入量的文本得出結論是,血漿濃度為12µmol/L足以實現正常的離體過氧化氫引起的溶血[3]。2014年的一篇評論把低於每公升9μmol定義為不足,每公升9-12µmol定義為邊緣值,而高於12µmol/L定義為足夠[23]。
血清濃度會隨年齡增長而增加。這歸因於維他命E在摻入脂蛋白的血液中循環,使血清脂蛋白濃度隨年齡增長而增加的事實。嬰兒和幼童低於不足的閾值有更高的風險[5]。囊性纖維化和其他脂肪吸收不良的情況可能導致血清維他命E降低。膳食補充劑可增加血清維他命E[3]。
膳食
建議每日攝取量
| 美國維他命E建議量(毫克/每天)[3] | |
|---|---|
| AI(0 - 6個月大嬰幼兒) | 4 |
| AI(7 - 12個月大嬰幼兒) | 5 |
| RDA(1 - 3歲兒童) | 6 |
| RDA(4 - 8歲兒童) | 7 |
| RDA(9 - 13歲兒童) | 11 |
| RDA(14 - 18歲青少年) | 15 |
| RDA (19歲以上成年人) | 15 |
| RDA(懷孕期婦女) | 15 |
| RDA(哺乳期婦女) | 19 |
| UL(成年人) | 1,000 |
維他命E的建議每日攝取量是根據α-生育酚形式而計算出來,因為它是最活躍或最可用的形式。當時,美國進行兩次全國調查、全國健康和營養考試調查(NHANES III 1988-91)和(1994 CSFII)的調查結果顯示,大部分美國人的飲食量無法提供足夠維他命E。
- 從食物中攝取維他命E的建議每日攝取量為15毫克,相等於22個IU的自然維他命E或33個IU的人工合成維他命E。
- 美國食品暨藥物管理局(FDA)對於維他命E的每日攝取建議量(RDA)僅僅20個IU至30個IU,其實20個IU或30個IU的維他命E攝取量可由食物中獲取。
- 因為標準多種維他命通常包含大約30個IU,需要另外一個維他命E補充去達到水平。
- 目前的指引認為每天補充超過1,000毫克的維他命E被認為不安全,等於1,500個IU自然來源維他命E,或1,100個IU的人工合成維他命E[24]。
美國國家醫學研究院於2000年更新了維他命E的參考膳食攝取量(EAR)和推薦膳食攝取量(RDA)[3]。RDA高於EAR,以便確定總額能夠覆蓋需求高於平均水平人群的量。當沒有足夠的信息來設置EAR和RDA時,則以足夠的攝入量(AI)來釐定。14歲及以上男女的維他命E的EAR為每天12毫克,RDA為每天15毫克[3]。為了安全起見,若證據充分的情況下,維他命和礦物質設定了容許攝入量上限(「上限」或參考膳食攝取量(UL))。對於12個月以下的嬰兒,其足夠的攝入量(AI)為每天4至5毫克。大鼠的出血性作用被選為關鍵終點以透過從最低可觀察到的不良反應水平(LOAEL)開始計算參考膳食攝取量,並通過不確定性因子計算來處理參考膳食攝取量。最終得出的結果是把參考膳食攝取量設置為每天1,000毫克[3]。估計平均需求量(EAR)、建議膳食許可量(RDA)、足夠的攝入量(AI)及參考膳食攝取量(UL)統稱為參考膳食攝取量(DRI)[3]。
歐洲食品安全局(EFSA)把這些信息的集合稱為膳食參考值,以人口參考攝入量(PRI)取代RDA,並以平均需求量代替EAR。AI和UL的定義與美國的相同。對於10歲及以上的男女,PRI值分別設定為每天11和13毫克,這些PRI值都低於美國的RDA[25]。懷孕期和哺乳期的PRI值為每天11毫克。對於1至9歲的兒童,PRI值從6毫克升高至9毫克[25]。EFSA使用對凝血功能的影響作為對安全性至關重要的影響。EFSA審查了相同的安全性問題,他們確定在一項人體試驗中未觀察到出現不良反應為每天540毫克,使用兩種不確定性因素得出的UL為270毫克,然後四捨五入為每天300毫克[26]。
日本國立衛生研究院設定的AI低於美國的RDA或歐盟的PRI及中間的UL:對於成年人AI,男性為每天7毫克,女性為每天6.5毫克,成年人的UL劑量為每天650–700毫克(女性),和每天750–900毫克(男性),具體數字取決於年齡[27]。印度建議每天攝入8至10毫克,並且沒有設定UL[28]。世界衛生組織建議成年人每天攝入10毫克[5],該攝入量低於政府的建議。
根據全球100多項研究的總結報告指,α-生育酚的平均攝入中位數為每天6.2毫克[5]。美國政府的調查結果顯示,成年女性的平均消秏量為每天8.4毫克,而成年男性的平均消秏量為每天10.4毫克[29]。兩者均低於RDA的每天15毫克。
食物標纖
對於美國食品和膳食補充劑標籤,每份的含量表示為每日數值的百分比(%DV)。用於維他命E的標籤中,每日數值的100%為30個IU,但該數值自2016年5月27日起被修訂為15毫克,以使它與RDA達成一致的協議[30][31]。截至2020年1月1日,對於每年食品銷售額超過1,000萬美元或以上的製造商必須遵守並符合更新的標籤法規,而每年食品銷售額不足1,000萬美元的製造商必須於2021年1月1日之前必須遵守更新的標籤法規[32][33][34]。在2020年1月1日履約日期之後的首六個月中,FDA計劃與製造商合作,以滿足新的營養成分標籤要求,並且在此期間將不會專注於針對這些要求的執法行動[32]。參考每日攝入量中提供了新舊成人每日數值的列表。
歐盟法規要求標籤上標明能量、蛋白質、脂肪、飽和脂肪、碳水化合物、糖和鹽。如果大量存在的話,可能會顯示出自願營養成分。其數量以參考攝入量(RI)的百分比而不是每日數值來顯示。對於維他命E來說,他們於2011年把100%的RI設定為12毫克[35]。
在1968-2016年,美國使用國際單位計算。1個IU相當於約0.667毫克的d(RRR)-α-生育酚(精確地為2/3毫克),或0.90毫克的dl-α-生育酚的生物等效量,對應於當時測量所得的立體異構體相對效力。2016年5月,他們對測量值進行了修訂,這樣使1毫克的維他命E相等於1毫克的d-α-生育酚,或是2毫克的dl-α-生育酚[36]。這種改變最初始於2000年,當時美國國家學院醫學院(IOM)從膳食計算中剔除了α-生育酚以外其他物質形成的維他命E。UL的數值不考慮作任何轉換[37]。歐洲食品安全局(EFSA)從未使用過IU作為單位,其測量僅考慮了RRR-α-生育酚[38]。
食物來源
美國農業部(USDA)的農業研究服務部維持著食物成分數據庫。最後一個主要修訂版本是2015年9月的第28版。除了表中顯示的自然來源外,某些即食穀物、嬰兒配方食品、液體營養產品和其他食品也都添加了α-生育酚[39]。
| 植物來源[39] | 數量 (毫克/每100克) |
|---|---|
| 小麥胚芽油 | 150 |
| 榛子油 | 47 |
| 菜籽油/西洋油菜的油 | 44 |
| 葵花籽油 | 41.1 |
| 杏仁油 | 39.2 |
| 紅花油 | 34.1 |
| 葡萄籽油 | 28.8 |
| 葵花籽仁 | 26.1 |
| 杏仁 | 25.6 |
| 杏仁奶油 | 24.2 |
| 穀物胚芽 | 19 |
| 植物來源[39] | 數量 (毫克/每100克) |
|---|---|
| 芥花籽油 | 17.5 |
| 棕櫚油 | 15.9 |
| 花生油 | 15.7 |
| 人造牛油 | 15.4 |
| 榛子 | 15.3 |
| 粟米油 | 14.8 |
| 橄欖油 | 14.3 |
| 大豆油 | 12.1 |
| 松子 | 9.3 |
| 花生醬 | 9.0 |
| 花生 | 8.3 |
| 食物來源[39] | 數量 (毫克/每100克) |
|---|---|
| 爆谷 | 5.0 |
| 蛋黃醬 | 3.3 |
| 開心果果仁 | 2.8 |
| 牛油果 | 2.6 |
| 菠菜(未經處理) | 2.0 |
| 蘆筍 | 1.5 |
| 西蘭花 | 1.4 |
| 腰果 | 0.9 |
| 麪包 | 0.2 - 0.3 |
| 糙米 | 0.2 |
| 馬鈴薯、意式麵食 | < 0.1 |
其他天然的維他命E來自:
補充劑

維他命E是脂溶性的,因此其膳食補充劑產品通常以維他命形式存在,以乙酸酯化合成生育酚乙酸酯,並溶於軟膠囊中的植物油中[1]。對於α-生育酚,每劑量的範圍從100到1,000個IU。較少的劑量會被摻入到多種維他命/礦物質片劑中。膳食補充劑公司也提供γ-生育酚和生育三烯酚的補充劑,後者是棕櫚油或是胭脂樹油的提取物。
副作用
減少補充劑的使用
1986年,在美國的女性保健專業人員使用維他命E補充劑的比例佔16.1%,1998年為46.2%,2002年為44.3%,但在2006年下降至19.8%。同樣,對於男性保健專業人員,同年的比率分別為18.9%、52.0%、49.4%和24.5%。研究筆者推測,在這些人群中減少使用可能是由於一些研究的出版物顯示維他命E補充劑毫無益處或帶來負面後果[44]。在美國軍事部門中,維他命處方予現役、預備役和退役軍人及其家屬,並於2007-2011年期間對他們進行了追踪,維他命E處方減少了53%,維他命C保持不變,而維他命D增加了454%[45]。美國的維他命E銷量報告顯示,2000年至2006年間的維他命E銷量下降了50%[46],可能的原因是一項綜合分析得出結論,認為維他命E與高劑量維他命E(以每天≥400個IU維持最少一年)相關,這也與全因死亡率增加有關[7]。
攝取過量
美國食品和營養委員會把根據動物模型得出的參考膳食攝取量(UL)設置為每天1,000毫克(1,500 IU),該模型顯示了高劑量時的出血情況[3]。歐洲食品安全局審查了相同的安全性問題,並將UL設定為每天300毫克[26]。一項長期臨床試驗的綜合分析報告指,當α-生育酚是唯一使用的補充劑時,全因死亡率非顯著的增加了2%。相同的綜合分析指,單獨使用α-生育酚或與其他營養素(維他命A、維他命C、β-胡蘿蔔素、硒)作組合使用時,其結果是統計上顯著增長了3%[6]。另一項綜合分析報告指,當α-生育酚是唯一的補充劑時,全因死亡率非顯著的增加了1%。分組分析報告表明天然(植物提取)或合成的α-生育酚之間沒有區別,或每天使用量是否少於或大於400個IU[47]。有報告指,在護膚產品中使用維他命E衍生物(例如護膚產品中的生育酚亞油酸酯和生育酚乙酸酯)會導致誘發過敏性接觸性皮炎,儘管其廣泛使用的發病率較低[48]。
一些報告中顯示其副作用很不常見,但由於它為脂溶性維他命,故容易造成累積。雖其副作用不常見,但它依然存在,而且過量攝取容易造成體內大量積聚,故應盡量避免長期過量攝取。
藥物相互作用
當從食物中攝入膳食維他命E的α-生育酚、其他生育酚和生育三烯酚的含量,似乎不會引起任何跟藥物的相互作用。膳食補充劑中α-生育酚的攝入量超過每天300毫克時,可能導致跟阿士匹靈、華法林、為諾瓦得士、環孢素產生相互作用,從而改變功能。對於阿士匹靈和華法林,大量的維他命E可能會增強抗血凝作用[4][49]。一項小型試驗證明,每天服用400毫克的維他命E會降低抗乳腺癌藥物泰莫西芬(Tamoxifen)的血藥濃度。在多項臨床試驗中,維他命E降低了免疫抑製劑環孢素A的血藥濃度[49]。
美國國家衛生院的膳食補充劑辦公室提出了一種憂慮,指維他命E可能會抵消抗癌放射療法的機制以及某些類型化學療法的作用,因此建議不要在這些患者群中使用。其引用的參考文獻指出減少治療不良反應但癌症存活率較差的情況,從而增加了透過治療保護腫瘤免受預期的氧化損傷的可能性[4]。
化學
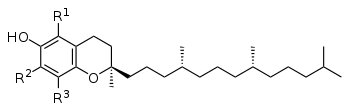

維他命E的營養成分是相當於100%的RRR-α-生育酚活性等效。那些貢獻α-生育酚活性的分子為是四種生育酚和四種生育三烯酚。生育酚主要有四種衍生物,按甲基位置分為α、β、γ和δ四種。對於生育三烯酚存在相同的構型中,除了疏水性側鏈具有三個碳-碳雙鍵,而生育酚則具有飽和的側鏈[50]。跟生育酚相關的化合物生育三烯酚在取代基不同時活性是一定的,但生育酚的活性會明顯降低。
那些貢獻α-生育酚活性的分子是四個生育酚和四個生育三烯酚,其中每個組別由四個前綴以α-、β-、γ-和δ-為標識的四個組別中。
對於α-生育酚的三個R中,每一個均具有一個連接的甲基(CH3);
對於β-生育酚:R1 = 甲基組,R2 = H,R3 = 甲基組;
對於γ-生育酚:R1 = H,R2 =甲基組,R3 =甲基組;
對於δ-生育酚:R1 = H,R2 = H,R3 =甲基組;
對於生育三烯酚存在相同的構型,除了疏水性側鏈外,它具有三個碳-碳雙鍵而生育酚具有飽和的側鏈[50]。
下表列出用以下官能團取代後生育三烯酚與生育酚的活性比:
| 衍生物 | R1 | R2 | R3 | 活性比(%) |
|---|---|---|---|---|
| α | CH3 | CH3 | CH3 | 100 |
| β | CH3 | H | CH3 | 40 |
| γ | H | CH3 | CH3 | 10 |
| δ | H | H | CH3 | 1 |
立體異構體
除了透過甲基的位置來區分生育酚和生育三烯酚外,生育酚還帶有一個帶著三個具有向右或向左方向的手性點或中心的植酸尾。α-生育酚的天然植物形式是RRR-α-生育酚,又稱為d-生育酚,而合成形式(所有外消旋全消旋維他命E,也是dl-生育酚)會隨著生物等效性的降低,其合成形式也是相等於八個立體異構體的RR,RRS,RSS,SSS,RSR,SRS,SRR和SSR的一部分,其生物等效性逐漸降低,因此1.36 mg的dl-生育酚被認為等同於d的1.0 mg -生育酚,天然形式。 換句話說,合成物具有天然藥效的73.5%[50]。
| Form | Structure |
|---|---|
| α-生育酚 | 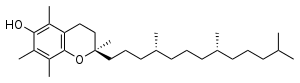 |
| β-生育酚 | 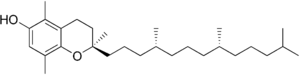 |
| γ-生育酚 | 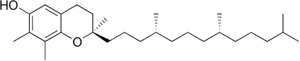 |
| δ-生育酚 | 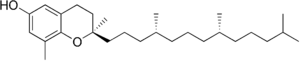 |
| 生育酚乙酸酯 | 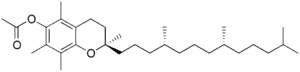 |
生育酚
α-生育酚是一種親脂性抗氧化劑,在穀胱甘肽過氧化物酶的途徑中起作用[51],它透過在脂質過氧化連鎖反應中產生的脂質自由基反應而氧化,從而保護細胞膜免受氧化[1][52]。這樣可以除去自由基中間體,並防止氧化反應繼續進行。在該過程中產生被氧化的α-生育酚自由基可通過其他抗氧化劑如抗壞血酸,視黃醇或泛醇等以有機氧化還原反應的還原形式循環回活性物質[53]。維他命E的其他形式也有其獨特的特性,例如:γ-生育酚是一種親核體,它可以與親電體突變原產生反應[11]。
生育三烯酚
四種生育三烯酚(α,β,γ,δ)在結構上跟四種生育酚相似,其主要區別在於前者俱有帶有三個碳-碳雙鍵的疏水側鏈,而生育酚則具有飽和的側鏈。對於α-生育三烯酚來說,三個「R」中的每一個均具有一個甲基(CH3)的連接。對於β-生育三烯酚來說,R1 = 甲基組,R2 = H,R3 =甲基組。對於γ-生育三烯酚來說,R1 = H,R2 = 甲基組,R3 = 甲基組。而對δ-生育三烯酚來說,R1 = H,R2 = H,R3 = 甲基組。棕櫚油是α-生育三烯酚和γ-生育三烯酚的良好來源[54]。
生育三烯酚只有單一手性中心,它在類異戊二烯尾部連接環的位置存在於2'苯甲酚環碳原子上。由於在這些部位的不飽和(C-C雙鍵),在相應的生育酚的植基尾部其它兩個相應的中心則不存在作為生育三烯酚手性中心。從植物中提取的生育三烯酚始終是右旋立體異構體,表示為d-生育三烯酚。從理論上說,也可以存在左旋形式的生育三烯酚(l-生育三烯酚),在分子的單個手性中心具有2S而不是2R的構型,但它跟合成的dl-α-生育酚不同,市面出售的生育三烯酚膳食補充劑都是從棕櫚油或胭脂紅油中提取的d-生育三烯酚。膳食補充生育三烯酚的初步臨床試驗表明其具有抗疾病活性的潛力[55]。
種類
幫助抗氧化最有效的維生素E是δ-生育酚,幫助抗不孕最有效的是α-生育酚。
粗分可分三種:
- 天然維他命E(d-α-生育酚)
- 半人造維他命E:d-α-生育酚醋酸酯,d-α-生育酚琥珀酸酯
- 人造/人工合成維生素E:dl-α-生育酚、dl-α-生育酚醋酸酯(一个d-α-生育酚分子与一个l-α-生育酚分子合成)
維他命E營養補充劑可分為六大類:
- 人造(人工合成)維生素E,“dl-α-生育酚”,作為醋酸鹽酯類,最廉價,通常最常被賣作營養補充劑
- 半人造“自然來源”維生素E酯類、由"自然來源" 加工成藥片藥丸及一粒有多種維他命的營養補充劑
- 高度鍊製的天然d-α-生育酚
- 低度鍊製的天然混雜數種的維他命E
- 高伽瑪維生素E營養補充丸
- 生育三烯酚(Tocotrienol)營養補充劑
化粧品及部分製藥用烟酸生育酚酯及亚油酸生育酚酯。
在健康人體内,半人造維生素E可主要在肝臟在幾天內被去酯化(de-esterified),但早產兒、年邁或不適的患者卻不能把人造及半人造維生素E去酯化。
代謝
生育三烯酚和生育酚(包括合成的α-生育酚的立體異構體),它們在膽酸、胰液和脂肪的存在時,在脂酶的作用下混合形成乳糜微粒,從小腸上部經非飽和的被動彌散方式被腸腔的上皮細胞吸收,並分泌到通往肝臟的肝門靜脈。各種形式的維他命E被吸收後大多由乳糜微粒攜帶經淋巴系統到達肝臟,其吸收效率估計為51%至86%[3],這適用於所有維他命E家族 — 在吸收過程中,維他命E跟其他維他命之間沒有區別。肝臟中的維他命E通過乳糜微粒和極低密度脂蛋白(VLDL)的載體作用進入血漿。乳糜微粒在血循環的分解過程中,將吸收的維他命E轉移進入脂蛋白循環,其他的作為乳糜微粒的殘骸。α-生育酚的主要氧化產物是α-生育醌,在脫去含氫的醛基生成葡糖醛酸。葡糖醛酸可通過膽汁排泄,或進一步在腎臟中被降解產生α-生育酸從尿酸中排泄。未經吸收的維他命E會通過糞便排出體外。此外,維他命E透過膽汁經肝臟排泄到腸腔,在那裡透過糞便重新吸收或排泄,並且所有維他命E都會被代謝,然後經尿液排出體外[3][50]。
到達肝臟後,RRR-α-生育酚優先被α-生育酚轉移蛋白(α-TTP)吸收。所有其他形式均被降解為2'-羧乙基-6-羥基苯並烷(CEHC),這個過程涉及截短分子的植酸尾部,然後進行硫酸化或醣醛酸化。這使分子具有水溶性,並讓它可經尿液排泄出來。α-生育酚也可通過相同的過程降解為2,5,7,8-四甲基-2-(2'-羧乙基)-6-羥基苯並二氫吡喃(α-CEHC),但速度較慢,因為它受到α-TTP的部分保護。大量攝入α-生育酚會導致尿液中的α-CEHC值升高,因此這似乎是處置過量維他命E的一種方法[3][50]。
α-生育酚轉移蛋白由8號染色體上的TTPA進行基因編碼。RRR-α-生育酚的結合位點是對親和力較低的β-,γ-或δ-生育酚來說是個疏水口袋,或具有對掌性2位的S構型的立體異構體。生育三烯酚的適應性也很差,因為其植酸尾中的雙鍵會形成一個剛性構型,這跟α-TTP口袋也不匹配[50]。儘管攝入了正常分量的維他命E,TTPA基因的罕見遺傳缺陷會導致人們表現出漸進的神經退行性疾病,這被稱為維他命E缺乏症的共濟失調(AVED)。這需要大量的α-生育酚作為膳食補充劑以彌補α-TTP的缺乏[21]。α-TTP的作用是將α-生育酚移動到肝細胞的質膜(肝細胞)上,在那裡可以將其整合到新創建的極低密度脂蛋白(VLDL)分子中。這些東西把α-生育酚傳送至身體其他部分的細胞。作為優先處理的結果的一個例子,美國於飲食中的γ-生育酚為每天攝入約70毫克,而血漿濃度約為2–5µmol/L;同時,飲食中的α-生育酚約為每天7毫克,但血漿濃度於每公升11-37µmol的範圍內[50]。
α-TTP對維他命E的維他命親和力[50]
| 維他命E複合物 | 親和力 |
|---|---|
| RRR-α-生育酚 | 100% |
| β-生育酚 | 38% |
| γ-生育酚 | 9% |
| δ-生育酚 | 2% |
| SSR-α-生育酚 | 11% |
| α-生育三烯酚 | 12% |
合成
生物合成
進行光合作用的植物、藻類和藍綠藻可合成生育酚。這是由四種生育酚和四種生育三烯酚組成化合物的化學家族;在營養方面,該化學家族被稱為維他命E。其生物合成從形成分子閉環部分的尿黑酸(HGA)開始。其側鏈連接(針對生育酚而言是飽和的,對於生育三烯酚而言是多不飽和),兩者的合成途徑是相同的,因此就可以創建γ-,然而中創建α-或Δ-,然後從β-化合物中生成[56][57]。生物合成發生在色素體之中[57]。
至於植物為何合成生育酚,其主要原因似乎是抗氧化活性。不同物種的植物和其不同部分是由不同的生育酚鉻醇所支配。其主要形式是存在於葉子中,因此綠色多葉蔬菜中的是α-生育酚[56]。其位置在於葉綠體的細胞膜中,以靠近進行光合作用[57]。其功能是為了保護免受陽光的紫外線輻射的損害。在正常的生長條件下,α-生育酚的存在似乎不是必不可少的,因為還有其他的光保護性化合物,通過突變失去合成α-生育酚能力的植物表現出正常的生長。然而,在乾旱、高溫或鹽誘導的氧化脅迫等緊張的生長條件下,若植物具有正常的合成能力,其生理狀態就更為優越[58]。
種子富含脂質,可為發芽期和早期生長提供能量。生育酚可以保護種子脂質免於氧化和變腐爛[56][57]。生育酚色素的存在延長了種子的壽命,並促進了成功的發芽和幼苗生長[58]。γ-生育酚在大多數植物物種的種子中佔主導地位,但也有例外。對於低芥酸菜子油、玉米油和大豆油,γ-生育酚的含量是高於α-生育酚的含量,但是對於紅花、葵花籽和橄欖油則恰恰相反[56][57][54]。在常用的食用油中,棕櫚油的獨特之處在於生育三烯酚的含量高於生育酚的含量[54]。種子生育酚含量還也取決於環境脅迫因素。例如,在杏仁中,乾旱或高溫會增加堅果中的α-生育酚和γ-生育酚的含量。在同一篇文章還提到乾旱會增加橄欖的生育酚含量,熱力對大豆也有同樣效果[59]。
工業合成
天然來源的d-α-生育酚可以從種子油中提取和純化,或γ-生育酚可以被提取、純化和甲基化以生成d-α-生育酚。對比從植物中提取的α-生育酚,也稱為d-α-生育酚,工業合成產生dl-α-生育酚。「它是由甲苯和2,3,5-三甲基對苯二酚的混合物合成的,在氯化氫氣體為催化劑的情況下,該混合物利用鐵跟異植醇反應生成『全外消旋α-生育酚』,並在氯化氫氣體的存在下利用鐵作為催化劑。該反應混合物以苛性鈉水溶液過濾並萃取。甲苯通過蒸發去除,其殘留物『全外消旋α-生育酚』通過真空蒸餾純化。」其成分規格的純度為>97%[60]。這種合成dl-α-生育酚含量具有d-α-生育酚大約50%的效力。對於人類或家養動物的膳食補充和強化食品的製造商會利用乙酸和琥珀酸把維他命的苯酚形式轉化為酯,因為這些酯在化學上更穩定,可提供更長的保質期。酯形式在腸道中被去酯化並作為游離的α-生育酚被吸收。
歷史
維他命E於1922年由赫伯特·麥克林·伊文斯及嘉芙蓮·畢曉普發現[13],他們在研究生殖過程中發現,一種脂溶性膳食因子對大白鼠的正常繁育必不可少,這種因子於1924年被命名為維他命E。在使用完全去除維他命E的飼料後可以引起大鼠的不孕症。在隨後的動物實驗中,研究人員發現,若小白鼠缺乏維他命E則會出現心、肝和肌肉退化以及不生育;而大鼠則雄性永久不生育,雌性不能懷上足月鼠胎,同時還有肝退化、心肌異常等症狀;猴子身上就會出現貧血、不生育、心肌異常。1935年,伊文斯及格拉迪斯·安德森·愛默生於加利福尼亞大學柏克萊分校以純淨形式把該物質首次分離出來[14],維他命E的結晶體於1936年被分離出來。由於維他命活性最初被確定為飲食中的生育因子(在大鼠中),所以它被命名為「生育酚(tocopherol)」是源自希臘語單詞「τόκος(出生)」及「φέρειν(承受或攜帶)」,總而言之其意思為「攜帶懷孕」,其「-ol」的結尾表示其狀態為化學醇。加利福尼亞大學的希臘文教授喬治·卡爾霍恩(George M. Calhoun)獲記為於命名過程中提供協助的人[15]。1938年,艾哈德·費爾霍茲闡明了其結構,此後不久的同年,瑞士化學家保羅·卡勒和他的團隊首先將其進行合成[61]。
1946年,維他命E在冠心病中的作用首次被提出[62][63]。隨後,同一研究小組進行了更多的心血管方面的工作[64],其中包括一項建議,即大劑量的維他命E可以減緩甚至逆轉動脈粥樣硬化的發展[65]。然而,2004年的一項綜合分析顯示,補充維他命E與心血管事件(非致命性中風或心肌梗塞)或心血管疾病死亡率之間並沒有關聯[66]。長期以來人們一直相信,局部應用含有維他命E的油有益於燒傷和傷口癒合[67],即使科學評論一再駁斥這一主張,這種信念仍然持續存在[9][68][69]。
在發現維他命E接近50年後,《美國醫學會雜誌》上的社論題為「尋找疾病的維他命」,其部分內容中讀到「...研究揭示了許多維他命的秘密,但沒有一定的治療用途,在人類中也沒有明確的缺乏症」。動物發現實驗指它是成功懷孕的必要條件,但是對於容易流產的婦女則沒有發現任何好處。血管健康的證據被認為令人信服的。該篇社論最後提到了一些初步預防幼兒溶血性貧血的人類證據[70]。
1980年代,研究人員發現,人類如果缺乏維他命E則會引發遺傳性疾病和代謝性疾病。隨著往後的深入研究,研究人員又認識到維他命E在預防心腦血管疾病、腫瘤、糖尿病及其他併發症、中樞神經系統疾病、運動系統疾病、皮膚疾病等各方面具有廣泛的作用。然而,在2004年的綜合分析顯示,維他命E補充劑跟心血管事件(非致命性中風或心肌梗塞)或心血管疾病死亡率之間並沒有關聯[71]。人們長期以來一直相信,局部使用含油的維他命E有益於燒傷和傷口癒合[67]。即使科學評論一再駁斥了這個主張,這主張依然存在[9][68][69]。
維他命E在嬰兒營養中的作用已有很長的研究歷史。從1949年開始,有一項針對早產兒進行的試驗表明,口服α-生育酚對水腫、顱內出血、溶血性貧血及早產兒視網膜病變具有保護作用[72]。2003年《考科藍》的一份評論報告得出結論,在早產嬰兒中補充維他命E可降低顱內出血和視網膜病變的風險,但注意到增加了敗血症的風險[73]。
参考文献
引用
- . Micronutrient Information Center, Linus Pauling Institute, Oregon State University, Corvallis, OR. 1 October 2015 [3 August 2019].
- Traber MG, Bruno RS. . BP Marriott, DF Birt, VA Stallings, AA Yates (编). . London, United Kingdom: Academic Press (Elsevier). 2020: 115–36. ISBN 978-0-323-66162-1.
- Institute of Medicine. . . Washington, DC: The National Academies Press. 2000: 186–283 [2020-08-25]. ISBN 978-0-309-06935-9. PMID 25077263. doi:10.17226/9810. (原始内容存档于2018-02-26).
- . Office of Dietary Supplements, US National Institutes of Health. 12 July 2019 [3 August 2019].
- Péter S, Friedel A, Roos FF, Wyss A, Eggersdorfer M, Hoffmann K, Weber P. . International Journal for Vitamin and Nutrition Research. December 2015, 85 (5–6): 261–281. PMID 27414419. doi:10.1024/0300-9831/a000281.
- Bjelakovic G, Nikolova D, Gluud C. . PLOS ONE. 2013, 8 (9): e74558. Bibcode:2013PLoSO...874558B. PMC 3765487. PMID 24040282. doi:10.1371/journal.pone.0074558.
- Miller ER, Pastor-Barriuso R, Dalal D, Riemersma RA, Appel LJ, Guallar E. . Annals of Internal Medicine. January 2005, 142 (1): 37–46. PMID 15537682. doi:10.7326/0003-4819-142-1-200501040-00110. 已忽略未知参数
|s2cid=(帮助) - Galli F, Azzi A, Birringer M, Cook-Mills JM, Eggersdorfer M, Frank J, 等. . Free Radical Biology & Medicine. January 2017, 102: 16–36. PMID 27816611. doi:10.1016/j.freeradbiomed.2016.09.017.
- Sidgwick GP, McGeorge D, Bayat A. . Archives of Dermatological Research. August 2015, 307 (6): 461–77. PMC 4506744. PMID 26044054. doi:10.1007/s00403-015-1572-0.
- Braunstein, Matthew H. . Nova Science Publishers. 1 March 2006: vii. ISBN 978-1-59454-971-7.
- Brigelius-Flohé R, Traber MG. . FASEB Journal. July 1999, 13 (10): 1145–55. PMID 10385606. doi:10.1096/fasebj.13.10.1145.
- Reboul E, Richelle M, Perrot E, Desmoulins-Malezet C, Pirisi V, Borel P. . Journal of Agricultural and Food Chemistry. November 2006, 54 (23): 8749–55. PMID 17090117. doi:10.1021/jf061818s.
- Evans HM, Bishop KS. . Science. December 1922, 56 (1458): 650–1. Bibcode:1922Sci....56..650E. JSTOR 1647181. PMID 17838496. doi:10.1126/science.56.1458.650.
- Oakes EH, , : 211–212, 2007, ISBN 978-1-4381-1882-6
- Evans HM; Emerson OH; Emerson GA. . Journal of Biological Chemistry. 1936, 113 (1): 319–332 [2020-08-25]. (原始内容存档于2007-09-29).
- Lide, David R. (编), 87th, Boca Raton, FL: CRC Press, 2006, ISBN 0-8493-0487-3
- Traber MG, Stevens JF. . Free Radical Biology & Medicine. September 2011, 51 (5): 1000–13. PMC 3156342. PMID 21664268. doi:10.1016/j.freeradbiomed.2011.05.017.
- Azzi A. . Molecular Aspects of Medicine. June 2018, 61: 92–103. PMID 28624327. doi:10.1016/j.mam.2017.06.004.
- Schneider C. . Molecular Nutrition & Food Research. January 2005, 49 (1): 7–30. PMID 15580660. doi:10.1002/mnfr.200400049.
- . WebMD. [2018-12-08] (中文(中国大陆)).
- Christopher Min K. . . Vitamins & Hormones 76. 2007: 23–43. ISBN 978-0-12-373592-8. PMID 17628170. doi:10.1016/S0083-6729(07)76002-8.
- Niki E, Traber MG. . Annals of Nutrition & Metabolism. 2012, 61 (3): 207–12. PMID 23183290. doi:10.1159/000343106.
- Traber MG. . Advances in Nutrition. September 2014, 5 (5): 503–14. PMC 4188222. PMID 25469382. doi:10.3945/an.114.006254.
- (PDF). 2017 [2020-08-24]. (原始内容 (PDF)存档于2017-08-28).
- (PDF), European Food Safety Authority, 2006 [2020-08-24], (原始内容 (PDF)存档于2016-03-16)
- Tanaka K, Terao J, Shidoh Y, Tamai H, Imai E, Okano T. . Journal of Nutritional Science and Vitaminology. 2013, 59: S57–S66. doi:10.3177/jnsv.59.S57.
- (PDF). [26 February 2018]. (原始内容 (PDF)存档于15 June 2016). 已忽略未知参数
|df=(帮助); 已忽略未知参数|url-status=(帮助) - (PDF). What We Eat In America, NHANES 2012–2014 (2016). [18 August 2018]. (原始内容存档 (PDF)于2017-02-24).
- (PDF). [2020-08-24]. (原始内容存档 (PDF)于2016-08-08).
- . Dietary Supplement Label Database (DSLD). [16 May 2020]. (原始内容存档于2020-04-07).
- . U.S. Food and Drug Administration (FDA). 30 December 2019 [16 May 2020].
 该来源属于公有领域,本文含有该来源内容。
该来源属于公有领域,本文含有该来源内容。 - . U.S. Food and Drug Administration (FDA). 27 May 2016 [16 May 2020]. (原始内容存档于2019-04-22).
 该来源属于公有领域,本文含有该来源内容。
该来源属于公有领域,本文含有该来源内容。 - . U.S. Food and Drug Administration (FDA). 21 December 2018 [16 May 2020].
 该来源属于公有领域,本文含有该来源内容。
该来源属于公有领域,本文含有该来源内容。 - . Official Journal of the European Union. 2011, 22 (11): 18–63 [2020-08-24]. (原始内容存档于2017-07-26).
- . National Institutes of Health. [2018-11-21].
- (PDF). USDA. February 2008. (原始内容 (PDF)存档于2012-02-19). 已忽略未知参数
|url-status=(帮助) - . EFSA Journal. July 2015, 13 (7). doi:10.2903/j.efsa.2015.4149.
only 2R-α-tocopherol stereoisomers were found to meet human requirements for the vitamin... Currently, only RRR-α-tocopherol is considered to be the physiologically active vitamer.
- . United States Department of Agriculture, Agricultural Research Service. Release 28. 2015 [18 August 2018]. (原始内容存档于2018-03-03).
- (PDF). World Health Organization. 2006 [18 August 2018]. (原始内容存档 (PDF)于2016-12-26).
- . Food Fortification Initiative, Enhancing Grains for Better Lives. [18 August 2018]. (原始内容存档于2017-04-04).
- . EFSA Journal. September 2015, 13 (9). doi:10.2903/j.efsa.2015.4247.
- . Food Additives and Ingredients Association UK & Ireland- Making life taste better. [27 October 2010]. (原始内容存档于1 June 2019). 已忽略未知参数
|url-status=(帮助) - Kim HJ, Giovannucci E, Rosner B, Willett WC, Cho E. . Journal of the Academy of Nutrition and Dietetics. March 2014, 114 (3): 436–43. PMC 3944223. PMID 24119503. doi:10.1016/j.jand.2013.07.039.
- Morioka TY, Bolin JT, Attipoe S, Jones DR, Stephens MB, Deuster PA. . Military Medicine. July 2015, 180 (7): 748–53. PMID 26126244. doi:10.7205/MILMED-D-14-00511.
- Tilburt JC, Emanuel EJ, Miller FG. . Journal of General Internal Medicine. September 2008, 23 (9): 1495–8. PMC 2518024. PMID 18618194. doi:10.1007/s11606-008-0704-z.
- Curtis AJ, Bullen M, Piccenna L, McNeil JJ. . Cardiovascular Drugs and Therapy. December 2014, 28 (6): 563–73. PMID 25398301. doi:10.1007/s10557-014-6560-7.
- Kosari P, Alikhan A, Sockolov M, Feldman SR. . Dermatitis. 2010, 21 (3): 148–53. PMID 20487657. doi:10.2310/6620.2010.09083. 已忽略未知参数
|s2cid=(帮助) - Podszun M, Frank J. . Nutrition Research Reviews. December 2014, 27 (2): 215–31. PMID 25225959. doi:10.1017/S0954422414000146.
- Manolescu B, Atanasiu V, Cercasov C, Stoian I, Oprea E, Buşu C. . Journal of Medicine and Life. 2008, 1 (4): 376–82. PMC 5654212. PMID 20108516.
- Wefers H, Sies H. . European Journal of Biochemistry. June 1988, 174 (2): 353–7. PMID 3383850. doi:10.1111/j.1432-1033.1988.tb14105.x.
- Traber MG, Atkinson J. . Free Radical Biology & Medicine. July 2007, 43 (1): 4–15. PMC 2040110. PMID 17561088. doi:10.1016/j.freeradbiomed.2007.03.024.
- Wang X, Quinn PJ. . Progress in Lipid Research. July 1999, 38 (4): 309–36. PMID 10793887. doi:10.1016/S0163-7827(99)00008-9.
- Shahidi F, de Camargo AC. . International Journal of Molecular Sciences. October 2016, 17 (10): 1745. PMC 5085773. PMID 27775605. doi:10.3390/ijms17101745.
- Meganathan P, Fu JY. . International Journal of Molecular Sciences. October 2016, 17 (11): E1682. PMC 5133770. PMID 27792171. doi:10.3390/ijms17111682.
- Mène-Saffrané L. . Antioxidants. December 2017, 7 (1): 2. PMC 5789312. PMID 29295607. doi:10.3390/antiox7010002.
- Fritsche S, Wang X, Jung C. . Antioxidants. December 2017, 6 (4): 99. PMC 5745509. PMID 29194404. doi:10.3390/antiox6040099.
- Falk J, Munné-Bosch S. . Journal of Experimental Botany. June 2010, 61 (6): 1549–66. PMID 20385544. doi:10.1093/jxb/erq030.
- Kodad O, Socias i Company R, Alonso JM. . Antioxidants. January 2018, 7 (1): 6. PMC 5789316. PMID 29303980. doi:10.3390/antiox7010006.
- . EFSA Journal. 2012, 10 (7): 2784. doi:10.2903/j.efsa.2012.2784.
- Karrer P, Fritzsche H, Ringier BH, Salomon H. . Nature. 1938, 141 (3580): 1057. Bibcode:1938Natur.141.1057K. doi:10.1038/1411057d0.
- Vogelsang A, Shute EV. . Nature. June 1946, 157 (3997): 772. Bibcode:1946Natur.157..772V. PMID 21064771. doi:10.1038/157772b0.
- Skelton F, Shute E, Skinner HG, Waud RA. . Science. June 1946, 103 (2687): 762. Bibcode:1946Sci...103R.762S. PMID 17836459. doi:10.1126/science.103.2687.762-b.
- Shute EV, Vogelsang AB. . Surgery, Gynecology & Obstetrics. January 1948, 86 (1): 1–8. PMID 18920873.
- Shute WE, Shute EV. Alpha Tocopherol (Vitamin E) in Cardiovascular Disease. Toronto, Ontario, Canada: Ryerson Press, 1954
- Eidelman RS, Hollar D, Hebert PR, Lamas GA, Hennekens CH. . Archives of Internal Medicine. July 2004, 164 (14): 1552–6. PMID 15277288. doi:10.1001/archinte.164.14.1552.
- Panin G, Strumia R, Ursini F. . Annals of the New York Academy of Sciences. December 2004, 1031 (1): 443–7. Bibcode:2004NYASA1031..443P. PMID 15753192. doi:10.1196/annals.1331.069. 已忽略未知参数
|s2cid=(帮助) - Tanaydin V, Conings J, Malyar M, van der Hulst R, van der Lei B. . Aesthetic Surgery Journal. September 2016, 36 (8): 959–65. PMID 26977069. doi:10.1093/asj/sjw046.
- Pehr K, Forsey RR. . CMAJ. November 1993, 149 (9): 1247–53. PMC 1485678. PMID 8221479.
- . JAMA: The Journal of the American Medical Association. 1967, 201 (3): 195–196. doi:10.1001/jama.1967.03130030065018.
- Eidelman RS, Hollar D, Hebert PR, Lamas GA, Hennekens CH. . Archives of Internal Medicine. July 2004, 164 (14): 1552–6. PMID 15277288. doi:10.1001/archinte.164.14.1552.
- Bell EF. . The American Journal of Clinical Nutrition. July 1987, 46 (1 Suppl): 183–6. PMID 3300257. doi:10.1093/ajcn/46.1.183.
- Brion LP, Bell EF, Raghuveer TS. . The Cochrane Database of Systematic Reviews. 2003, (4): CD003665. PMID 14583988. doi:10.1002/14651858.CD003665.
来源
- Institute of Medicine, Food and Nutrition board. Dietary Reference Intakes: Vitamin C, Vitamin E, Selenium, and Carotenoids. National Academy Press, Washington, DC, 2000.
- U.S. Department of Agriculture, Agricultural Research Service, 1999. USDA Nutrient Database for Standard Reference, Release 13. Nutrient Data Laboratory Home Page, https://web.archive.org/web/20060105045324/http://www.nal.usda.gov/fnic/foodcomp/
- Dietary Guidelines Advisory Committee, Agricultural Research Service, United States Department of Agriculture (USDA). Report of the Dietary Guidelines Advisory Committee on the Dietary Guidelines for Americans, 2000. https://web.archive.org/web/20031204191827/http://www.ars.usda.gov/dgac/
- Rosenberg H and Feldzamen AN. The book of vitamin therapy. New York: Berkley Publishing Corp, 1974.
- Papas, A., (1999). The Vitamin E Factor, Harper Collins Publishers, Inc.
- Rolfes, S,R., Pinna, K., & Whitney, E., (2012). Understanding Normal and Clinical Nutrition, 9th ed. Belmont, CA: Wadsworth Cengage Learning
外部連結
- Vitamin E CAS No is 59-02-9
- US Office of Dietary Supplements article on Vitamin E 页面存档备份,存于
- Vitamin E (Tocopherols and Tocotrienols)
- Vitamin E risk assessment 页面存档备份,存于, Expert Group on Vitamins and Minerals, , 2003
- High dose vitamin E leads to longer more active lives in mice
- Scientifically-proven benefits of regular vitamin e consumption
- Harvard School of Public Health Nutrition Source
