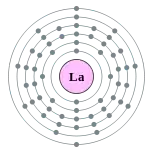
镧
鑭,是一種化學元素,元素符號為La,原子序數為57。是一種柔軟、具有韌性、質地為銀白色的金屬,暴露在空氣中時會慢慢失去光澤。鑭非常柔軟,可以直接用刀切割。元素週期表中鑭和鎦之間的一組15個相似元素,稱作鑭系元素,其中鑭是排序中的第一個。 鑭有時也被認為是第6週期第3族的過渡金屬的第一個元素,而鎦也是第3族元素。 所有的鑭屬於稀土元素。通常氧化態為+3。 鑭在人體沒有扮演任何生物角色,但對某些特定細菌來說,它非常重要。鑭對人體沒有特別的毒性,但顯示出一些抗菌活性。 鑭通常伴隨著鈰或是其他稀土元素出現。在1839年首次由瑞典化學家Carl Gustav Mosander在硝酸鈰中發現的雜質,因此命名為鑭,來自古希臘語λανθάνειν (lanthanein),意為“隱藏”。 雖然鑭被歸類為稀土元素,但鑭在地殼中元素含量的排名為第28,幾乎是鉛的三倍。 在獨居石和氟碳鈰礦等礦物中佔鑭元素含量的四分之一[1]。直到1923年終於從這些複雜的礦物中成功提取出純鑭金屬。 鑭化合物可作為多種用途,如催化劑、玻璃添加劑、用於影室燈或投影機的碳弧燈、打火機及火炬中的點火元件、陰極射線管、閃爍體、 GTAW電極或其他用品。在腎衰竭的情況下,碳酸鑭可作為磷酸鹽結合劑。
性质
物理性质
镧是一种柔软,有延展性的银白色金属具有六角形在室温下的晶体结构。 在310℃,镧变化为面心立方结构,以及在865℃下变成体心立方结构。 镧容易被氧化(一厘米大小的样品将完全在一年内氧化),因此用于以元素形式仅用于研究目的。 例如,单个镧原子已被分离,通过注入成富勒烯分子。如果碳纳米管填充有那些镧封装富勒烯并退火,镧金属纳米串链是碳纳米管内产生的。
化学性质
镧具有两个氧化态,三价和二价,前者稳定性更强。 例如,LaH3比LaH2更稳定。镧容易燃烧,在150 ℃下 ,以形成镧(III)的氧化物 :
- 4La + 3O2 → 2La2O3
然而,当在室温下暴露于潮湿的空气中,氧化镧,氧化形成氧化物水合物具有大量的增加。
镧与在冷水中缓慢腐蚀,热水中加快,以形成氢氧化镧:
- 2La(s)+6H2O(l)→2La(OH)3(aq)+3H2(g)
镧可以和所有卤素反应,如果温度高於200℃,则反应较剧烈
- 2La(s)+3F2(g)→2LaF3(s)
- 2La(s)+3Cl2(g)→2LaCl3(s)
- 2La(s)+3Br2(g)→2LaBr3(s)
- 2La(s)+3I2(g)→2LaI3(s)
镧结合与氮,碳,硫,磷,硼,硒,硅和砷在高温下,形成二元化合物。 无色的La3+离子的结构等同于氙的构型。
同位素
镧天然存在的同位素共有2种,分别为镧-138和镧-139,其中只有镧-139稳定,镧-138半衰期较长。
用途
高折射耐鹼玻璃、鑭鎳五:氫氣儲藏裝置、電池電極、相機鏡片、石油裂解催化劑、打火石
外部連結
- 元素镧在洛斯阿拉莫斯国家实验室的介紹(英文)
- —— {{LinkForElement|La| }}(英文)
- 元素镧在The Periodic Table of Videos(諾丁漢大學)的介紹(英文)
- 元素镧在Peter van der Krogt elements site的介紹(英文)
- WebElements.com – {{LinkForElement|La| }}(英文)